کاربردهای سلولهای بنیادی
مقدمه :
جايگزين كردن سلولهاي بيمار با سلولهاي سالم را سلولدرماني مينامند و مانند فرايند جايگزين كردن اندام است؛ البته، در اينجا به جاي اندام تنها از سلولها بهره ميگيرند. برخي بيماريها و آسيبها را ميتوان با جايگزين اندام سالمي درمان كرد، اما اندوختهي اندامها اهدايي بسيار اندك است. سلولهاي بنيادي ميتوانند سرچشمهي جايگزين و نوشدني از سلولهاي تخصصيافته باشند. بهتازگي، پژوهشگران بهرهگيري از سلولهاي بنيادي جنيني و بالغ را به عنوان خاستگاه گونههاي سلولي تخصصيافته، مانند سلولهاي عصبي، سلولهاي ماهيچهاي، سلولهاي خون و سلولهاي پوست، برسي ميكنند تا آنها را براي درمان بيماريهاي گوناگون به كار برند.
براي مثال، در بيماري پاركينسون، سلولهاي بنيادي ممكن است براي پديدآوردن گونهي ويژهاي از سلولها عصبي، سلولهايي كه دوپامين آزاد ميكنند، به كار آيند. اكنون در ميدان نظر، اين سلولهاي عصبي را ميتوان در بدن بيمار كار گذاشت و آنها در آنجا شبكهي عصبي را در بخش آسيبديده از نو سيمكشي خواهند كرد و كاركرد آن بخش را به آن بازميگردانند و بنابراين، بيمار را درمان ميكنند. برخی از این کاربردها شامل موارد زیر می شود:
آناند اسواروپ، محقق سلول بنيادي در موسسه ملي چشم و يکي از اعضاي موسسههاي ملي سلامت آمريکا گفت: «اين کشف نشانگر قابليت فوقالعاده تحقيقات سلولهاي بنيادي در درمان گستره وسيعي از بيماريهاي مرگبار و ناتوان کننده است که ميليونها انسان را مبتلا کرده است.»
محققان در آزمايشگاه، سلولهاي بنيادي را به سلولهاي شبه نرون تبديل کردند و سپس آنها را به گوش داخلي خوکچههاي هندي پيوند زدند. سه ماه بعد اين خوکچهها بخشي از شنوايي خود را به دست آوردند. هدف از انجام اين مطالعه، رشد مجدد سلولهاي حساس شنوايي اعلام شده است. اين سلولها نقش حياتي در قدرت شنوايي پستانداران دارند. با اين وجود محققان هنوز نميدانند چگونه اين فرآيند اتفاق ميافتد. محققان در يک کنفرانس مطبوعاتي، هدف نهايي از انجام اين تحقيقات را، مطالعات مشابه روي انسان اعلام کردند. هنگاميکه سلولهاي حساس شنوايي در گوش داخلي انسان و ساير پستانداران در اثر صداي بلند، بيماريهاي خودايمني، داروهاي سمي و يا پيري ميميرند، آسيب دايمي به شنوايي وارد ميشود. در اين ميان پرندگان و خزندگان خوش شانسترند. سلولهاي شنوايي آسيب ديده در اين حيوانات، باززايي کردند و قدرت شنوايي حيوان را بازگرداندند. در يک مطالعه ديگر، مايکل زوبر و همکارانش در دانشگاه پزشکي ساني در نيويورک با استفاده از سلولهاي بنيادي، در جنين نابيناي قورباغه، چشمهاي سالم توليد کردند. معمولا سلولهاي بنيادي قورباغه در محيط آزمايشگاه فقط به پوست تبديل ميشوند اما گروه زوبر هفت عامل ژنتيکي مختلف را که موجب فعال شدن ژنهاي تشکيل دهنده چشم ميشوند، به ظرف آزمايش خود اضافه کردند.
زوبر گفت: «هنگاميکه سلولهاي تغيير يافته به جنين قورباغه پيوند زده شد، نوزادان قورباغه، ميتوانستند ببينند. آزمايشهاي ژنتيکي نشان داده است سلولهاي بنيادي به انواع بسيار متفاوت سلولها تبديل ميشوند.» با اين وجود وي تاکيد کرد که نتيجه اين مطالعه هنوز روي انسان کاربردي ندارد. وي افزود: «هدف پزشکي باززايي، توليد مجدد انواع مختلف سلولها است.»
اخيراً دانشمندان انگليسي، توانستهاند به کمک سلولهاي بنيادي، حس بينايي را به موشهاي نابينا برگردانند.
اين موفقيت گامي به سوي درمان بسياري از افراد نابينا محسوب ميشود؛ هرچند كه از درمان موشهاي كور تا درمان انسانهاي نابينا هنوز فاصله زيادي وجود دارد.
دانشمندان انگليسي موفق شدهاند حيواناتي را که چشم آنها در اثر بيماريهاي مشابه آنچه در انسان ديده ميشود آسيب ديده، معالجه کنند. آنها با پيوند زدن سلولهاي بنيادي شبکيه به چشم اين حيوانات نابينا موفق به اين کار شدهاند.
محققان ميگويند اگر از نتايج اين دستاورد بتوان براي معالجه بيماريهاي چشم انسان استفاده کرد، ميليونها نفر که مبتلا به انواع مختلف بيماريهاي شبکيه چشم هستند - از مشکلات ناشي از سالمندي گرفته تا ديابت - از آن بهره خواهند برد، چرا که پيش از اين ترميم سلولهاي شبکيه چشم امکان نداشت.
شبکيه چشم، لايهاي از سلولهاي عصبي و حساس به نور مخروطي و استوانهاي است که تصاوير را به پيامهاي عصبي تبديل ميکند و به دليل داشتن ماهيت عصبي، در صورت آسيب ديدگي ترميم نميشود.
اصولاً ترميم سلولهاي عصبي بطور طبيعي در بدن انسان بهصورت بسيار محدود انجام ميشود. ميتوان گفت سلولهاي عصبي يا همان «نورون»ها تقريباً غير قابل ترميم تلقي ميشوند و ازهمين روست كه مثلاً يك بيمار دچار ضايعه نخاعي را نميتوان بهآساني درمان كرد.
به اين دلايل است كه گامي، هرچند كوچك، در ترميم سلولهاي عصبي، ميتواند موفقيت بزرگي تلقي شود. در مطالعه اخير، که با بودجه شوراي تحقيقات پزشکي انگلستان انجام شده، دانشمندان موسسه تحقيقات چشم و بهداشت کودک وابسته به دانشگاه لندن و بيمارستان چشم مورفيلدز، سلولهايي را که از رشد بيشتري برخوردار بودند و از قبل براي تبديل شدن به دريافت کنندههاي نوري برنامهريزي شده بودند را به چشم موشهاي نابينا پيوند زدند.
تيم پزشکان، سلولهاي بنيادي مورد نياز در اين پيوند را از موشهاي پنج روزه، يعني زماني که شبکيه شکل ميگيرد، برداشتند. اين سلولها سپس به چشم حيواناتي که از لحاظ ژنتيکي طوري طراحي شده بودند که مبتلا به بيماري چشمي شوند و به تدريج بينايي خود را از دست بدهند، پيوند زده شد.
پيوند موفق بود. سلولهاي بنيادي به سلولهاي شبکيه تبديل شده و سلولهاي تازه شبکيه به ساير سلول هاي عصبي شبکيه پيوند خوردند و به اين ترتيب حس بينايي دوباره به موشهاي نابينا شده بازگشت.
آزمايشها نشان داد که مردمک چشم موش به نور واکنش نشان داد و عصب چشم فعال بود و ثابت ميكرد علائم به مغز ارسال ميشود.
دانشمندان ميگويند شايد شبکيه يکي از بهترين نقاط براي امتحان کردن پيوند سلولي باشد، زيرا نابودي دريافت کنندههاي نوري در ابتدا به باقي بخشهاي عصبي ميان چشم و مغز آسيب نميرساند.
تلاشهاي قبلي براي پيوند زدن سلولهاي بنيادي، به اين اميد که به دريافت کنندههاي نوري تبديل شوند، شکست خورده بود، چرا که سلولها از رشد کافي برخوردار نبودند.
با وجودي که نتايج اين کار در موشها خيلي خوب جواب داده ولي تکرار کاري مشابه آن در انسان کمي مشکل است و البته اين مشکل، بيشتر اخلاقي است، چرا که براي اينکه بتوان از سلولهاي بنيادي انسان در مرحلهاي كه در حال تبديل به سلولهاي شبکيه است، استفاده کرد، بايد سلولهاي بنيادي از جنين در سه ماه دوم بارداري برداشته شود.
به همين خاطر، گروه تحقيقاتي دانشگاه لندن و بيمارستان چشم پزشکي مورفيلدز قصد ندارد در اين مسير حرکت کند.
دکتر رابرت مک لارن، متخصص در بيمارستان چشم مورفيلدز که در اين تحقيقات شرکت داشته در اين باره ميگويد: «اکنون، هدف مطالعه سلولهاي بنيادي بزرگسالان است تا معلوم شود آيا امکان تغيير ژنتيکي آنها به طوري که مانند سلولهاي شبکيه موش رفتار کنند وجود دارد يا نه؟»
سلولهايي در حاشيه شبکيه چشم افراد بزرگسال وجود دارد که تصور ميشود داراي خواص سلولهاي بنيادي باشد و به گفته تيم متخصصان اين پروژه تحقيقاتي، ميتواند براي عمل پيوند مفيد باشد.
طبق اعلام سازمان جهانى بهداشت (WHO) تعداد زوج هاي نابارور دنيا به 510 ميليون زوج مي رسد. با اين حال، ايران در سال هاي اخير در درمان ناباروري حرف هاي زيادي براي گفتن داشته است.
باز شدن پاي تحقيقات مربوط به سلول هاي بنيادي هم در اين ميان، دريچه تازه اي است كه شايد به زودي به روي جماعت در انتظار فرزند گشوده شود. محققان ايراني اميدوارند با پيوند سلول هاي بنيادي به افراد نابارور قابليت به وجود آمدن نطفه در آن ها را به وجود مي آورند.
محمدرضا نوروزي رئيس انجمن ناباروري ايران، ميگويد: "يكي از روشهاي جديد درمان ناباروري استفاده از سلولهاي بنيادي براي مردان و زناني است كه توانايي توليد نطفه ندارند. آزمايشهاي مطالعات حيواني اين روش در ايران بر روي موش انجام شده و موفقيتآميز بوده است. فاز انساني مطالعه اين روش هم شروع شده كه اگر به جواب نهايي برسد، تحول مهمي در درمان ناباروري محسوب ميشود."
بر اساس مطالعات انجام شده، 90 درصد زوجهاي نابارور ميتوانند با استفاده از يكي از روشهاي درماني موجود صاحب فرزند شوند. استفاده از سلولهاي بنيادي ميتواند مشكل 10 درصد باقيمانده را حل كند."
شيوع ناباروري
در حال حاضر، روشهاي درماني مختلفي براي درمان ناباروري در ايران و جهان وجود دارد. لقاح مصنوعي، IVF و ميترواينجكشن از جمله اين روش ها هستند كه به گفته درمانگران به طور معمول تا حدود 35درصد در درمان ناباروري مؤثرند.
روش تخمكگذاري و لقاح مصنوعي معمولا به تولد چند جنين منتهي ميشود. در حالي كه زوجهاي نابارور معمولا خواهان يك فرزند هستند و اين يكي از عوارض اين نوع درمانها است كه در برخي كشورها مانند چين با توجه به سياست كشورشان محدوديتهايي براي اين روش قائل شده اند. البته اين مسئله در كشور ما هنوز بلاتكليف است.
به گفته رئيس انجمن ناباروري ايران، در دنياي امروز عوامل مختلفي موجب ناباروري در مردان و زنان مي شود كه علاوه بر عوامل ژنتيك عوامل اجتماعي، زندگي شهري، برخورد با اشعهها، بيماري هاي عفوني شايع جوامع، در اين زمينه دخيل هستند.
تئوريهايي كه مبني بر تأثير آلودگي هوا و امواج موبايل در اين زمينه مطرح است كه هنوز اثبات نشده است.
عوامل روحي رواني هم موجب ناتواني جنسي و كم شدن ارتباط جنسي ميشود كه در اين زمينه دخيل هستند. علاوه بر اين بالا رفتن سن ازدواج موجب شده است كه شانس ناباروري در زوج هاي جوان افزايش يابد.
علت از بین رفتن گروه خاصی از نورون ها در بیماری پاركینسون نامشخص است لیكن گمان می رود تنش ناشی از حضور اكسیژن (oxidative stress)، عملكرد نادرست میتوكندری و excytotoxic damage در فیزیوپاتولوژی این بیماری مؤثر باشند؛ در ضمن به دلیل اینكه این بیماری در اغلب موارد به صورت انفرادی (sporadic) است، گمان می رود فاكتورهای ژنتیكی همراه با فاكتورهای محیطی نظیر ویروسها در بروز این بیماری نقش ایفا می كنند. در عین حال موارد نادری از این بیماری به صورت خانوادگی وجود دارد. در این موارد جهش در ژن های خاصی كه عمدتاً در تجزیه پروتیین ها نقش دارند، عامل اصلی بروز بیماری است. رایج ترین روش درمانی این بیماری استفاده از داروهای L-Dopa و Carbidopa است. این دو ماده سبب افزایش سنتز و رهاسازی دوپامین می شوند در رفع كم تحركی و سختی، به ویژه در مراحل اولیه درمان مؤثر هستند.
اما با پیشرفت بیماری به دلیل از بین رفتن نورون های دوپامینرژیك سنتز دوپامین، نتیجتاً كارآیی درمان كاهش می یابد. به تازگی روش جدید سلول درمانی برای درمان این بیماران مورد توجه قرار گرفته است. در این روش، درمان با پیوند سلولهای مناسب به ناحیه آسیب دیده صورت می گیرد. بدین منظور می توان انواع مختلی از سلول ها از جمله بافت مغزی جنین را به كار برد. لیكن به دلیل مشكلات اخلاقی و تكنیكی موجود به دلیل نیاز به تعداد زیاد جنین و نیز رد پیوند استفاده از این روش با محدودیت های زیاد روبرو است.گزینه دیگر برای سلول درمانی استفاده از سلولهای بنیادی (stem cell) است. به منظور كاربرد این سلولها در پیوند و درمان بیماری پاركینسون لازم است این سلولها ابتدا به نورون های دوپامینرژیك تمایز یابند. با دو روش كلی می توان به این هدف نایل شد: ۱) دستكاری ژنتیكی سلولهای بنیادی ۲)تغییر شرایط محیط كشت سلولهای بنیادی. در روش اول با واردكردن ژنی كه نقش اساسی در تكوین نورون های دوپامینرژیك دارد ( نظیر فاكتور رونویسی Nurrl) به سلولهای بنیادی، تمایز این سلولها را به نورون های دوپامینرژیك موجب می شویم.
در روش دوم با اضافه كردن فاكتورهای القاكننده خاص به محیط كشت و از طریق كشت همراه (coculture) سلولهای بنیادی با گروه خاصی از سلولها كه توانایی القای سلول بنیادی به سلولهای عصبی را دارند نورون های دوپامینرژیك حاصل می شود. فاكتورهایی كه جهت القا استفاده می شوند عمدتاً برگرفته از مسیرهای تكوینی طبیعی تولید این نورون ها در بدن است و از آن جمله می توان فاكتورهای Shh و FGF۸ را نام برد. شناسایی نورون های دوپامینرژیك براساس داشتن آنزیم (TH) Tyrosine Hydroxylase صورت می گیرد. TH آنزیم اصلی در مسیر تولید دوپامین از اسید آمینه Tyrosine است. پس از تولید سلولهای بیان كننده این آنزیم، این سلولها به موش مدل پاركینسونی تزریق می شوند. چنین موشی با وارد كردن آسیب بافتی به ناحیه خاصی از مغز میانی (midstriaTum) به وسیله تزریق ماده (۶-OHD hyroxydopamine) حاصل می شود. گروه دیگری ازمحققان از سلولهای بنیادی تمایز نیافته جهت پیوند استفاده كرده اند. این سلولها پس از پیوند به ناحیه آسیب دیده، به نورون های دوپامینرژیك تمایز می یابند. با این حال در هر دو نوع آزمایش مشكلاتی در زمینه تعیین تعداد دقیق سولهای پیوند شده و احتمال تشكیل تومور و مرگ سلولهای پیوند شده وجود دارد. لذا با وجود تحقیقات صورت گرفته، هنوز مطالعات بیشتری به منظور ارزیابی كارایی و ایمنی پیوند سلولهای بنیادی جهت درمان بیماران پاركینسونی نیاز است
6)روش جديدي براي پيوند سلولهاي بنيادي به بيماران قلبي با استفاده از نانوتكنولوژي
استفاده از سلولهاي بنيادي براي درمان بيماريهاي صعبالعلاج، يكي از اميدهاي در حال تحقق بشر در حوزة علوم پزشكي است كه روزبهروز، افقهاي تازهاي از آن نمايان ميشود. در مطلب حاضر كه گزيدهاي از سخنان دكتر عليرضا قدسيزاد، رزيدنت سال پنجم جراحي قلب در دانشگاه دوسلدورف آلمان است، به روش جديدي از پيوند سلولهاي بنيادي بالغ به بيماران قلبي اشاره شده است كه در آن از نانوتكنولوژي هم استفاده ميشود. وي اين روش را بهعنوان پروژة تحقيقاتي براي اتمام دورة تخصصي جراحي قلب انجام داده است:
استفاده از سلولهاي بنيادي براي درمان بيماريهاي صعبالعلاج، يكي از اميدهاي در حال تحقق بشر در حوزة علوم پزشكي است كه روزبهروز، افقهاي تازهاي از آن نمايان ميشود. در مطلب حاضر كه گزيدهاي از سخنان دكتر عليرضا قدسيزاد، رزيدنت سال پنجم جراحي قلب در دانشگاه دوسلدورف آلمان است، به روش جديدي از پيوند سلولهاي بنيادي بالغ به بيماران قلبي اشاره شده است كه در آن از نانوتكنولوژي هم استفاده ميشود. وي اين روش را بهعنوان پروژة تحقيقاتي براي اتمام دورة تخصصي جراحي قلب انجام داده است:
در اين روش جديد كه نوعي Stem cell therapy (درمان با استفاده از سلولهاي بنيادي) است و نيازمند انجام عمل قلب باز است، ابتدا با استفاده از نور ليزر، بافت عضلاني قلب بيمار در ناحية دچار ايسكمي تحريك ميشوند. سپس، سلولهاي بنيادي اخذشده از خود فرد به اطراف ناحية دچار آسيب تزريق ميشوند تا ضمن تمايز به سلولهاي عضلة قلب، منطقة آسيبديده را ترميم نمايند.
لازم به ذكر است كه در اين روش، نمونه مغز استخوان، پس از بيهوشي بيمار در اتاق عمل و از استخوانهاي لگن تهيه ميشود. حجم نمونة مغز استخوان گرفتهشده در اين مرحله فاكتور مهمي است كه تعداد نهايي سلولهاي بنيادي ACC133 + را تعيين ميكند. گروه جراحي ما تاكنون بيشترين مقدار گزارششدة مغز استخوان (حدود 330 ميليليتر) در دنيا را از بيمار اخذ كرده است. پس از اين مرحله، سلولهاي بنيادي مورد نظر با استفاده از كيت خاصي از نمونة آسپيرة مغز استخوان جداسازي ميشود و به روش ترانس اپيكارديال (از بيرون عضلة قلبي) به نقاط متعدد اطراف ناحية ايسكميك تزريق ميشود.
1- با توجه به اينكه كلية مراحل استخراج و پيوند سلولهاي بنيادي در مدت زمان حدود 3 ساعت قابل انجام است، بنابراين مدت ماندن بيمار در اتاق عمل بهطور قابل ملاحظهاي كوتاهتر است.
2- استفاده از كيت ويژة جداسازي سلولهاي بنيادي در يك سيستم بسته و استريل، عملاً نياز به آزمايشگاههاي مجهز و پيشرفته با استانداردهاي خاص ( GMP Lab ) را مرتفع ميكند. اين كار با بالابردن ضريب ايمني كار، احتمال انتقال آلودگي و عفونت به بيمار را منتفي ميسازد.
3- تمام مراحل تهية نمونه مغز استخوان، جداسازي سلولها و پيوند آنها، در اتاق عمل و صرفاً توسط خود جراح قلب صورت ميگيرد. بنابراين، با استفاده از اين شيوه نيازي به همكاري گروه ديگري از متخصصان مانند هماتولوژيستها و غيره نيست.
4- با توجه به اينكه در اين روش علاوه بر تزريق سلولهاي بنيادي به اطراف عضلة دچار عارضه، از خاصيت همافزايي نور ليزر نيز استفاده ميشود، در نتيجة التهاب موقت ايجادشدة ناشي از تابش نور ليزر، خونرساني به ناحية ايسكميك و تزريقشده، افزايش مييابد و با اين كار، احتمال موفقيت در پيوند سلولهاي بنيادي و زنده ماندن سلولهاي پيوندي افزايش مييابد.
شايان ذكر است كه در بيش از 50 درصد بيماران قلبي، قبل از اقدام به عمل جراحي معيارهاي لازم براي پيوند سلولهاي بنيادي وجود دارد. اما با اين روش، در مورد بيماران ديگري كه در حالت اورژانس به بيمارستان منتقل شده و اين تشخيص قبلاً براي آنها داده نشده باشد، ميتوان پس از اقدام به عمل جراحي و در حين كار چنين تصميمي را اتخاذ كرد. براي مثال، اگر بيماراني كه در مرحلة نهايي نارسايي قلبي ( End stage heart failure ) قرار داشته و به علت سختشدن ديواره عروق كرونري، رگهاي درگير بهطور كامل بستهشده و به موقع تحت درمان بايپس قرار نگيرند، جراح تنها پس از باز كردن قفسة سينه بيمار متوجه عدم كارايي روش بايپس براي درمان فرد ميشود. در چنين موارد اورژانسي، ميتوان با پيوند سريع سلولهاي بنيادي به قلب بيمار، جان او را نجات داد.
لازم به ذكر است كه در داخل نمونة اخذشدة مغز استخوان، كمتر از 5/1 درصد سلولها از نوع ACC133 + هستند و بقيه شامل ردههاي ديگر سلولي هستند. براي مثال، كمتر از 10 درصد سلولها از نوع CD34 + و حدود 25-20 درصد سلولها CD117 + هستند.
توليد اينترفرونها در زمان خود، انقلاب در پزشكي محسوب شد و اين اميدواري را پيش آورد كه بتواند بهعنوان درمان قطعي سرطان مورد استفاده قرار گيرد؛ اما گذشت زمان برخي محدوديتهاي آن را نمايان ساخت.
پس از آن، ژندرماني به عنوان راهي براي درمان سرطان مطرح شد كه سر و صداي زيادي در مجامع علمي و پزشكي به راه انداخت؛ در اين تكنولوژي، معمولاً از ويروسها به عنوان ناقلين ژنها استفاده ميشود كه مشكلاتي همچون تومورزايي، بيماريزايي و غيره را به همراه دارد و لذا اين روش نيز با محدوديتهاي جدي روبرو شد.
امروزه يكي از كاربردهاي سلولهاي بنيادي كه توجه زيادي را به خود معطوف داشته است، همين درمان سرطان است؛ چرا كه از سلولهاي بنيادي انساني و معمولاً بدون تغيير ژنتيكي، ميتوان براي ترميم بافتهاي آسيب ديده استفاده كرد.
هر چند استفاده از سلولهاي بنيادي، در مراحل اوليه خود به سر ميبرد، اما متخصصين معتقدند در آيندهاي نهچندان دور، كاربردهاي وسيعي در علم پزشكي خواهد داشت. با اين اعتقاد، هماكنون در اقصي نقاط جهان تحقيقات وسيعي در خصوص استفاده از سلولهاي بنيادي در جهت تأمين سلامت انسان در حال انجام است. در ذيل به چند نمونه از كاربردهاي نزديك به حصول سلولهاي بنيادي اشاره ميشود:
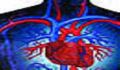
1- ترميم بافتهاي آسيبديده قلب
امروزه شمار زيادي از مردم دنيا از بيماريهاي قلبي ناشي از آ?سيبديدگي بافتهاي آن رنج ميبرند كه بعضاً منجر به مرگ نيز ميشود. ترميم بافتهاي آسيبديده، همواره يكي از دغدغههاي پزشكان و متخصصين علوم پزشكي بوده و بهرهگيري از سلولهاي بنيادي، اميد تازهاي در اين عرصه به وجود آورده است. متخصصين اميدوارند سلولهاي بنيادي را از مغز استخوان افراد بيمار (يا جنين نوظهور) استخراج و آنها را در محيط آزمايشگاه به سلولهاي قلبي تبديل نمايند و نهايتاً با تزريق اين سلولهاي تمايزيافته به بدن، امكان ترميم بافتهاي آسيبديده قلب را فراهم آورند.
البته اين تكنيك هنوز در مرحله آزمايشگاهي است، اما موفقيتهاي بهدست آمده در حيوانات آزمايشگاهي، احتمال بهرهگيري از آن را در انسان قوت بخشيده است.
2- ترميم بافتهاي استخواني
در افرادي كه شكستگي وسيع استخوان دارند و يا كساني كه مورد عمل جراحي مغزي قرار گرفته و كاسه سر آنها برداشته شده و همچنين اشخاصي كه استخوانهاي آنها بهكندي جوش ميخورد، از سلولهاي بنيادي براي جوشخوردگي سريع و جلوگيري از عفونتهاي بعدي استفاده ميشود. در اين تكنيك، سلولهاي بنيادي مزانشيمي از فرد گرفته شده و در محيط آزمايشگاه به سلولهاي استئوپلاست (استخواني) تبديل ميشوند، سپس اين سلولها در كنار بافتهاي آسيبديده استقرار مييابند تا باعث جوشخوردگي سريع اين بافتها گردند. در اين مورد، سلولها از خود شخص جدا ميشوند؛ بنابراين مشكل پسزدگي و عوارض جانبي را نيز در برندارد.
تكنيك مذكور از مرحله آزمايشگاهي خارج شده و هماكنون دركشورهاي پيشرفته دنيا از جمله آمريكا و ژاپن به طور عملي و كاربردي بر روي بيماران انجام ميشود.
3- درمان بيماريها و ضايعات عصبي
پيشرفتهاي بشر در زمينه توليد، تكثير و تمايز سلولهاي بنيادي، اين اميد را به وجود آورده است كه بتوان از اين سلولها در مداواي ضايعات عصبي مانند قطع نخاع و بيماريهاي عصبي همچون آلزايمر، پاركينسون، MS و غيره نيز بهره برد. در اين مورد نيز پس از تهيه سلولهاي بنيادي از شخص موردنظر، آنها را به سلول عصبي تبديل نموده و براي ترميم يا مداوا مورد استفاده قرار ميدهند. البته بخش اعظم اين تكنولوژي، در مرحله آزمايشگاهي است؛ اما با پيشرفتهاي خوبي همراه بوده است. بهعنوان مثال، طي گزارشي كه اخيراً منتشره شده، متخصصين فرانسوي موفق شدند با استفاده از سلولهاي مزانشيمي، موش قطع نخاع شدهاي را تا حدي بهبود بخشند كه قادر به حركت باشد ( البته نه با تعادل صددرصد). اين موضوع در صورتيكه با موفقيت نهايي توأم شود، انقلاب بزرگي در پزشكي به شمار ميرود.
ضمن اينكه يك شركت آمريكايي بنام اورسي كه يك مركز تحقيقاتي خصوصي بوده و متخصصين ارشد جهان در زمينه سلولهاي بنيادي را گرد هم آورده، ادعا كرده است كه قادر به مداواي بيماريهايي مانند آلزايمر، پاركينسون، MS و غيره ميباشد كه اين عمل را با استفاده از سلولهاي بنيادي خود شخص انجام ميدهد؛ البته در قبال آن هزينههاي بالايي تا حد 100 هزار دلار دريافت مينمايند.
4- ترميم سوختگيها و ضايعات پوستي
جراحات پوستي ناشي از سوختگي يا صدمات ديگر، بسياري از بيماران را به خود مبتلا نموده است. در روش معمول براي ترميم قسمتهاي صدمهديده، از پوست بخشهاي سالم بدن استفاده ميشود كه مشكلاتي را براي بيمار بهوجود ميآورد. اما با .استفاده از سلولهاي بنيادي ميتوان سلولهاي پوستي را در محيط آزمايشگاه توليد نمود و درترميم بافتهاي صدمهديده از آنها استفاده كرد. اين تكنولوژي در حال حاضر، كاربردي شده و توسط يكي از بيمارستانهاي انگلستان مورد استفاده قرار ميگيرد.
5- ترميم لوزالمعده (پانكراس) و ترشح انسولين
اخيراً در دانشگاه آلبرتا كانادا، متخصصين موفق شدند سلولهاي بنيادي مزانشيمي را به سلولهاي پانكراس انساني تبديل نمايند و به بيماران ديابتي منتقل نمايند. اين آزمايش بر روي 23 نفر انجام شد كه 16 نفر از تزريق انسولين بينياز شدند. يادآوري ميشود كه اين پيوند از نوع اتولوگ بود (براي مداواي هر شخص از سلولهاي بنيادي خود وي استفاده شد) و مشكلات جانبي در بر نداشت.
6- آزمون تأثير داروهاي جديد
داروهاي سنتتيك جديد ممكن است بر سلولها يا بافتهاي انساني تأثيرات متفاوتي داشته باشند كه امكان تست آنها در انسانها به دليل مسايل اخلاق پزشكي وجود ندارد. بهعنوان مثال، يك داروي سنتتيك قلبي ممكن است بر سلولها يا بافتهاي قلبي تأثير سويي داشته باشد. در اين موارد ميتوان سلولهاي قلبي يا هر بافت ديگر را با استفاده از سلولهاي بنيادي توليد نمود و داروهاي جديد را بر روي آنها آزمايش كرد، بدون اينكه نياز به آزمايش در بدن انسان باشد (آزمايشات مقدماتي انساني). در اين خصوص سلولهاي بنيادي جنيني ميتوانند كاربرد وسيعي داشته باشند.
7- ترميم ساير بافتهاي آسيبديده
مواردي كه اشاره شد كاربردهايي از سلولهاي بنيادي بود كه به صورت كاربردي درآمده بودند و يا نزديك به كاربردي شدن هستند، اما از كاربردهاي بالقوه اين سلولها ميتوان به ترميم بافتهاي آسيب ديده ديگر بدن از جمله غضروف، كبد، ماهيچه و غيره اشاره كرد كه ميتواند دامنه كاربرد سلولهاي بنيادي را در آينده افزايش دهد.
يك نكته مهم
در اطلاعرساني عمومي كاربرد سلولهاي بنيادي، بايد به اين نكته توجه شود كه انتظارات بيش از حد توانايي اين تكنولوژي در مردم به وجود نيايد. ساخت اندام، يكي از اميدهايي است كه ممكن است در برخي از مردم ايجاد گردد؛ بايد خاطر نشان كرد. كه با دانش كنوني بشر، امكان توليد عضو يا اندام توسط اين تكنولوژي وجود ندارد و به نظر نميرسد در آيندهاي نزديك نيز اين امر محقق شود. بهعنوان مثال، اگر قلب را در نظر بگيريم علاوه بر شكل آن كه در كاركردش بسيار حايز اهميت است، از سلولها و بافتهاي مختلفي از جمله بافت ماهيچهاي، خوني، اپيدرمي، رگ و غيره درست شده است. اگر بخواهيم سلولهاي بنيادي را به هر يك از اين بافتها تبديل نماييم، نيازمند اعمال شرايط و تيمارهاي ويژهاي هستيم كه فراهم كردن همه آنها به طور همزمان در يك بيورآكتور غيرممكن است. شايد در آينده بشر بتواند اين اعضاء را دربدن انسان يا حيوان توليد نمايد كه بهويژه در مورد دوم علاوه بر مشكلات تكنيكي با محدوديتهاي اخلاقي نيز مواجه است.
با اين تفاسير، كاربرد قابل انتظار بهرهگيري از سلولهاي بنيادي در شرايط فعلي و آينده نزديك، ترميم بافتهاي آسيبديده است كه در موارد فوق به آنها اشاره شد. هر چند همين كاربردها نيز در صورت فراگيرشدن، انقلابي در پزشكي محسوب ميشوند.
سلولهاي بنيادي چه كاربردهايي ميتواند داشته باشد؟
جايگزين كردن سلولهاي بيمار با سلولهاي سالم را سلولدرماني مينامند و مانند فرايند جايگزين كردن اندام است؛ البته، در اينجا به جاي اندام تنها از سلولها بهره ميگيرند. برخي بيماريها و آسيبها را ميتوان با جايگزين اندام سالمي درمان كرد، اما اندوختهي اندامها اهدايي بسيار اندك است. سلولهاي بنيادي ميتوانند سرچشمهي جايگزين و نوشدني از سلولهاي تخصصيافته باشند. بهتازگي، پژوهشگران بهرهگيري از سلولهاي بنيادي جنيني و بالغ را به عنوان خاستگاه گونههاي سلولي تخصصيافته، مانند سلولهاي عصبي، سلولهاي ماهيچهاي، سلولهاي خون و سلولهاي پوست، برسي ميكنند تا آنها را براي درمان بيماريهاي گوناگون به كار برند.
براي مثال، در بيماري پاركينسون، سلولهاي بنيادي ممكن است براي پديدآوردن گونهي ويژهاي از سلولها عصبي، سلولهايي كه دوپامين آزاد ميكنند، به كار آيند. اكنون در ميدان نظر، اين سلولهاي عصبي را ميتوان در بدن بيمار كار گذاشت و آنها در آنجا شبكهي عصبي را در بخش آسيبديده از نو سيمكشي خواهند كرد و كاركرد آن بخش را به آن بازميگردانند و بنابراين، بيمار را درمان ميكنند. برخی از این کاربردها شامل موارد زیر می شود:
1)سلولهاي بنيادي، قدرت شنوايي و بينايي را در حيوانات برميگردانند
آناند اسواروپ، محقق سلول بنيادي در موسسه ملي چشم و يکي از اعضاي موسسههاي ملي سلامت آمريکا گفت: «اين کشف نشانگر قابليت فوقالعاده تحقيقات سلولهاي بنيادي در درمان گستره وسيعي از بيماريهاي مرگبار و ناتوان کننده است که ميليونها انسان را مبتلا کرده است.»
محققان در آزمايشگاه، سلولهاي بنيادي را به سلولهاي شبه نرون تبديل کردند و سپس آنها را به گوش داخلي خوکچههاي هندي پيوند زدند. سه ماه بعد اين خوکچهها بخشي از شنوايي خود را به دست آوردند. هدف از انجام اين مطالعه، رشد مجدد سلولهاي حساس شنوايي اعلام شده است. اين سلولها نقش حياتي در قدرت شنوايي پستانداران دارند. با اين وجود محققان هنوز نميدانند چگونه اين فرآيند اتفاق ميافتد. محققان در يک کنفرانس مطبوعاتي، هدف نهايي از انجام اين تحقيقات را، مطالعات مشابه روي انسان اعلام کردند. هنگاميکه سلولهاي حساس شنوايي در گوش داخلي انسان و ساير پستانداران در اثر صداي بلند، بيماريهاي خودايمني، داروهاي سمي و يا پيري ميميرند، آسيب دايمي به شنوايي وارد ميشود. در اين ميان پرندگان و خزندگان خوش شانسترند. سلولهاي شنوايي آسيب ديده در اين حيوانات، باززايي کردند و قدرت شنوايي حيوان را بازگرداندند. در يک مطالعه ديگر، مايکل زوبر و همکارانش در دانشگاه پزشکي ساني در نيويورک با استفاده از سلولهاي بنيادي، در جنين نابيناي قورباغه، چشمهاي سالم توليد کردند. معمولا سلولهاي بنيادي قورباغه در محيط آزمايشگاه فقط به پوست تبديل ميشوند اما گروه زوبر هفت عامل ژنتيکي مختلف را که موجب فعال شدن ژنهاي تشکيل دهنده چشم ميشوند، به ظرف آزمايش خود اضافه کردند.
زوبر گفت: «هنگاميکه سلولهاي تغيير يافته به جنين قورباغه پيوند زده شد، نوزادان قورباغه، ميتوانستند ببينند. آزمايشهاي ژنتيکي نشان داده است سلولهاي بنيادي به انواع بسيار متفاوت سلولها تبديل ميشوند.» با اين وجود وي تاکيد کرد که نتيجه اين مطالعه هنوز روي انسان کاربردي ندارد. وي افزود: «هدف پزشکي باززايي، توليد مجدد انواع مختلف سلولها است.»
2)درمان نابینایی با سلولهاي بنيادي
اخيراً دانشمندان انگليسي، توانستهاند به کمک سلولهاي بنيادي، حس بينايي را به موشهاي نابينا برگردانند.
اين موفقيت گامي به سوي درمان بسياري از افراد نابينا محسوب ميشود؛ هرچند كه از درمان موشهاي كور تا درمان انسانهاي نابينا هنوز فاصله زيادي وجود دارد.
دانشمندان انگليسي موفق شدهاند حيواناتي را که چشم آنها در اثر بيماريهاي مشابه آنچه در انسان ديده ميشود آسيب ديده، معالجه کنند. آنها با پيوند زدن سلولهاي بنيادي شبکيه به چشم اين حيوانات نابينا موفق به اين کار شدهاند.
محققان ميگويند اگر از نتايج اين دستاورد بتوان براي معالجه بيماريهاي چشم انسان استفاده کرد، ميليونها نفر که مبتلا به انواع مختلف بيماريهاي شبکيه چشم هستند - از مشکلات ناشي از سالمندي گرفته تا ديابت - از آن بهره خواهند برد، چرا که پيش از اين ترميم سلولهاي شبکيه چشم امکان نداشت.
شبکيه چشم، لايهاي از سلولهاي عصبي و حساس به نور مخروطي و استوانهاي است که تصاوير را به پيامهاي عصبي تبديل ميکند و به دليل داشتن ماهيت عصبي، در صورت آسيب ديدگي ترميم نميشود.
اصولاً ترميم سلولهاي عصبي بطور طبيعي در بدن انسان بهصورت بسيار محدود انجام ميشود. ميتوان گفت سلولهاي عصبي يا همان «نورون»ها تقريباً غير قابل ترميم تلقي ميشوند و ازهمين روست كه مثلاً يك بيمار دچار ضايعه نخاعي را نميتوان بهآساني درمان كرد.
به اين دلايل است كه گامي، هرچند كوچك، در ترميم سلولهاي عصبي، ميتواند موفقيت بزرگي تلقي شود. در مطالعه اخير، که با بودجه شوراي تحقيقات پزشکي انگلستان انجام شده، دانشمندان موسسه تحقيقات چشم و بهداشت کودک وابسته به دانشگاه لندن و بيمارستان چشم مورفيلدز، سلولهايي را که از رشد بيشتري برخوردار بودند و از قبل براي تبديل شدن به دريافت کنندههاي نوري برنامهريزي شده بودند را به چشم موشهاي نابينا پيوند زدند.
تيم پزشکان، سلولهاي بنيادي مورد نياز در اين پيوند را از موشهاي پنج روزه، يعني زماني که شبکيه شکل ميگيرد، برداشتند. اين سلولها سپس به چشم حيواناتي که از لحاظ ژنتيکي طوري طراحي شده بودند که مبتلا به بيماري چشمي شوند و به تدريج بينايي خود را از دست بدهند، پيوند زده شد.
پيوند موفق بود. سلولهاي بنيادي به سلولهاي شبکيه تبديل شده و سلولهاي تازه شبکيه به ساير سلول هاي عصبي شبکيه پيوند خوردند و به اين ترتيب حس بينايي دوباره به موشهاي نابينا شده بازگشت.
آزمايشها نشان داد که مردمک چشم موش به نور واکنش نشان داد و عصب چشم فعال بود و ثابت ميكرد علائم به مغز ارسال ميشود.
دانشمندان ميگويند شايد شبکيه يکي از بهترين نقاط براي امتحان کردن پيوند سلولي باشد، زيرا نابودي دريافت کنندههاي نوري در ابتدا به باقي بخشهاي عصبي ميان چشم و مغز آسيب نميرساند.
تلاشهاي قبلي براي پيوند زدن سلولهاي بنيادي، به اين اميد که به دريافت کنندههاي نوري تبديل شوند، شکست خورده بود، چرا که سلولها از رشد کافي برخوردار نبودند.
با وجودي که نتايج اين کار در موشها خيلي خوب جواب داده ولي تکرار کاري مشابه آن در انسان کمي مشکل است و البته اين مشکل، بيشتر اخلاقي است، چرا که براي اينکه بتوان از سلولهاي بنيادي انسان در مرحلهاي كه در حال تبديل به سلولهاي شبکيه است، استفاده کرد، بايد سلولهاي بنيادي از جنين در سه ماه دوم بارداري برداشته شود.
به همين خاطر، گروه تحقيقاتي دانشگاه لندن و بيمارستان چشم پزشکي مورفيلدز قصد ندارد در اين مسير حرکت کند.
دکتر رابرت مک لارن، متخصص در بيمارستان چشم مورفيلدز که در اين تحقيقات شرکت داشته در اين باره ميگويد: «اکنون، هدف مطالعه سلولهاي بنيادي بزرگسالان است تا معلوم شود آيا امکان تغيير ژنتيکي آنها به طوري که مانند سلولهاي شبکيه موش رفتار کنند وجود دارد يا نه؟»
سلولهايي در حاشيه شبکيه چشم افراد بزرگسال وجود دارد که تصور ميشود داراي خواص سلولهاي بنيادي باشد و به گفته تيم متخصصان اين پروژه تحقيقاتي، ميتواند براي عمل پيوند مفيد باشد.
4)درمان ناباروري با سلولهاي بنيادي
طبق اعلام سازمان جهانى بهداشت (WHO) تعداد زوج هاي نابارور دنيا به 510 ميليون زوج مي رسد. با اين حال، ايران در سال هاي اخير در درمان ناباروري حرف هاي زيادي براي گفتن داشته است.
باز شدن پاي تحقيقات مربوط به سلول هاي بنيادي هم در اين ميان، دريچه تازه اي است كه شايد به زودي به روي جماعت در انتظار فرزند گشوده شود. محققان ايراني اميدوارند با پيوند سلول هاي بنيادي به افراد نابارور قابليت به وجود آمدن نطفه در آن ها را به وجود مي آورند.
محمدرضا نوروزي رئيس انجمن ناباروري ايران، ميگويد: "يكي از روشهاي جديد درمان ناباروري استفاده از سلولهاي بنيادي براي مردان و زناني است كه توانايي توليد نطفه ندارند. آزمايشهاي مطالعات حيواني اين روش در ايران بر روي موش انجام شده و موفقيتآميز بوده است. فاز انساني مطالعه اين روش هم شروع شده كه اگر به جواب نهايي برسد، تحول مهمي در درمان ناباروري محسوب ميشود."
بر اساس مطالعات انجام شده، 90 درصد زوجهاي نابارور ميتوانند با استفاده از يكي از روشهاي درماني موجود صاحب فرزند شوند. استفاده از سلولهاي بنيادي ميتواند مشكل 10 درصد باقيمانده را حل كند."
شيوع ناباروري
در حال حاضر، روشهاي درماني مختلفي براي درمان ناباروري در ايران و جهان وجود دارد. لقاح مصنوعي، IVF و ميترواينجكشن از جمله اين روش ها هستند كه به گفته درمانگران به طور معمول تا حدود 35درصد در درمان ناباروري مؤثرند.
روش تخمكگذاري و لقاح مصنوعي معمولا به تولد چند جنين منتهي ميشود. در حالي كه زوجهاي نابارور معمولا خواهان يك فرزند هستند و اين يكي از عوارض اين نوع درمانها است كه در برخي كشورها مانند چين با توجه به سياست كشورشان محدوديتهايي براي اين روش قائل شده اند. البته اين مسئله در كشور ما هنوز بلاتكليف است.
به گفته رئيس انجمن ناباروري ايران، در دنياي امروز عوامل مختلفي موجب ناباروري در مردان و زنان مي شود كه علاوه بر عوامل ژنتيك عوامل اجتماعي، زندگي شهري، برخورد با اشعهها، بيماري هاي عفوني شايع جوامع، در اين زمينه دخيل هستند.
تئوريهايي كه مبني بر تأثير آلودگي هوا و امواج موبايل در اين زمينه مطرح است كه هنوز اثبات نشده است.
عوامل روحي رواني هم موجب ناتواني جنسي و كم شدن ارتباط جنسي ميشود كه در اين زمينه دخيل هستند. علاوه بر اين بالا رفتن سن ازدواج موجب شده است كه شانس ناباروري در زوج هاي جوان افزايش يابد.
5)کاربرد سلولهای بنیادی در بیماری پارکینسون
علت از بین رفتن گروه خاصی از نورون ها در بیماری پاركینسون نامشخص است لیكن گمان می رود تنش ناشی از حضور اكسیژن (oxidative stress)، عملكرد نادرست میتوكندری و excytotoxic damage در فیزیوپاتولوژی این بیماری مؤثر باشند؛ در ضمن به دلیل اینكه این بیماری در اغلب موارد به صورت انفرادی (sporadic) است، گمان می رود فاكتورهای ژنتیكی همراه با فاكتورهای محیطی نظیر ویروسها در بروز این بیماری نقش ایفا می كنند. در عین حال موارد نادری از این بیماری به صورت خانوادگی وجود دارد. در این موارد جهش در ژن های خاصی كه عمدتاً در تجزیه پروتیین ها نقش دارند، عامل اصلی بروز بیماری است. رایج ترین روش درمانی این بیماری استفاده از داروهای L-Dopa و Carbidopa است. این دو ماده سبب افزایش سنتز و رهاسازی دوپامین می شوند در رفع كم تحركی و سختی، به ویژه در مراحل اولیه درمان مؤثر هستند.
اما با پیشرفت بیماری به دلیل از بین رفتن نورون های دوپامینرژیك سنتز دوپامین، نتیجتاً كارآیی درمان كاهش می یابد. به تازگی روش جدید سلول درمانی برای درمان این بیماران مورد توجه قرار گرفته است. در این روش، درمان با پیوند سلولهای مناسب به ناحیه آسیب دیده صورت می گیرد. بدین منظور می توان انواع مختلی از سلول ها از جمله بافت مغزی جنین را به كار برد. لیكن به دلیل مشكلات اخلاقی و تكنیكی موجود به دلیل نیاز به تعداد زیاد جنین و نیز رد پیوند استفاده از این روش با محدودیت های زیاد روبرو است.گزینه دیگر برای سلول درمانی استفاده از سلولهای بنیادی (stem cell) است. به منظور كاربرد این سلولها در پیوند و درمان بیماری پاركینسون لازم است این سلولها ابتدا به نورون های دوپامینرژیك تمایز یابند. با دو روش كلی می توان به این هدف نایل شد: ۱) دستكاری ژنتیكی سلولهای بنیادی ۲)تغییر شرایط محیط كشت سلولهای بنیادی. در روش اول با واردكردن ژنی كه نقش اساسی در تكوین نورون های دوپامینرژیك دارد ( نظیر فاكتور رونویسی Nurrl) به سلولهای بنیادی، تمایز این سلولها را به نورون های دوپامینرژیك موجب می شویم.
در روش دوم با اضافه كردن فاكتورهای القاكننده خاص به محیط كشت و از طریق كشت همراه (coculture) سلولهای بنیادی با گروه خاصی از سلولها كه توانایی القای سلول بنیادی به سلولهای عصبی را دارند نورون های دوپامینرژیك حاصل می شود. فاكتورهایی كه جهت القا استفاده می شوند عمدتاً برگرفته از مسیرهای تكوینی طبیعی تولید این نورون ها در بدن است و از آن جمله می توان فاكتورهای Shh و FGF۸ را نام برد. شناسایی نورون های دوپامینرژیك براساس داشتن آنزیم (TH) Tyrosine Hydroxylase صورت می گیرد. TH آنزیم اصلی در مسیر تولید دوپامین از اسید آمینه Tyrosine است. پس از تولید سلولهای بیان كننده این آنزیم، این سلولها به موش مدل پاركینسونی تزریق می شوند. چنین موشی با وارد كردن آسیب بافتی به ناحیه خاصی از مغز میانی (midstriaTum) به وسیله تزریق ماده (۶-OHD hyroxydopamine) حاصل می شود. گروه دیگری ازمحققان از سلولهای بنیادی تمایز نیافته جهت پیوند استفاده كرده اند. این سلولها پس از پیوند به ناحیه آسیب دیده، به نورون های دوپامینرژیك تمایز می یابند. با این حال در هر دو نوع آزمایش مشكلاتی در زمینه تعیین تعداد دقیق سولهای پیوند شده و احتمال تشكیل تومور و مرگ سلولهای پیوند شده وجود دارد. لذا با وجود تحقیقات صورت گرفته، هنوز مطالعات بیشتری به منظور ارزیابی كارایی و ایمنی پیوند سلولهای بنیادی جهت درمان بیماران پاركینسونی نیاز است
6)روش جديدي براي پيوند سلولهاي بنيادي به بيماران قلبي با استفاده از نانوتكنولوژي
استفاده از سلولهاي بنيادي براي درمان بيماريهاي صعبالعلاج، يكي از اميدهاي در حال تحقق بشر در حوزة علوم پزشكي است كه روزبهروز، افقهاي تازهاي از آن نمايان ميشود. در مطلب حاضر كه گزيدهاي از سخنان دكتر عليرضا قدسيزاد، رزيدنت سال پنجم جراحي قلب در دانشگاه دوسلدورف آلمان است، به روش جديدي از پيوند سلولهاي بنيادي بالغ به بيماران قلبي اشاره شده است كه در آن از نانوتكنولوژي هم استفاده ميشود. وي اين روش را بهعنوان پروژة تحقيقاتي براي اتمام دورة تخصصي جراحي قلب انجام داده است:
استفاده از سلولهاي بنيادي براي درمان بيماريهاي صعبالعلاج، يكي از اميدهاي در حال تحقق بشر در حوزة علوم پزشكي است كه روزبهروز، افقهاي تازهاي از آن نمايان ميشود. در مطلب حاضر كه گزيدهاي از سخنان دكتر عليرضا قدسيزاد، رزيدنت سال پنجم جراحي قلب در دانشگاه دوسلدورف آلمان است، به روش جديدي از پيوند سلولهاي بنيادي بالغ به بيماران قلبي اشاره شده است كه در آن از نانوتكنولوژي هم استفاده ميشود. وي اين روش را بهعنوان پروژة تحقيقاتي براي اتمام دورة تخصصي جراحي قلب انجام داده است:
هدف از پيوند
در اين روش جديد كه نوعي Stem cell therapy (درمان با استفاده از سلولهاي بنيادي) است و نيازمند انجام عمل قلب باز است، ابتدا با استفاده از نور ليزر، بافت عضلاني قلب بيمار در ناحية دچار ايسكمي تحريك ميشوند. سپس، سلولهاي بنيادي اخذشده از خود فرد به اطراف ناحية دچار آسيب تزريق ميشوند تا ضمن تمايز به سلولهاي عضلة قلب، منطقة آسيبديده را ترميم نمايند.
سلولهاي بنيادي مورد استفاده و شيوة عمل
لازم به ذكر است كه در اين روش، نمونه مغز استخوان، پس از بيهوشي بيمار در اتاق عمل و از استخوانهاي لگن تهيه ميشود. حجم نمونة مغز استخوان گرفتهشده در اين مرحله فاكتور مهمي است كه تعداد نهايي سلولهاي بنيادي ACC133 + را تعيين ميكند. گروه جراحي ما تاكنون بيشترين مقدار گزارششدة مغز استخوان (حدود 330 ميليليتر) در دنيا را از بيمار اخذ كرده است. پس از اين مرحله، سلولهاي بنيادي مورد نظر با استفاده از كيت خاصي از نمونة آسپيرة مغز استخوان جداسازي ميشود و به روش ترانس اپيكارديال (از بيرون عضلة قلبي) به نقاط متعدد اطراف ناحية ايسكميك تزريق ميشود.
استفاده از ليزر بهعنوان عامل تقويتكننده
مزاياي اين روش پيوند
1- با توجه به اينكه كلية مراحل استخراج و پيوند سلولهاي بنيادي در مدت زمان حدود 3 ساعت قابل انجام است، بنابراين مدت ماندن بيمار در اتاق عمل بهطور قابل ملاحظهاي كوتاهتر است.
2- استفاده از كيت ويژة جداسازي سلولهاي بنيادي در يك سيستم بسته و استريل، عملاً نياز به آزمايشگاههاي مجهز و پيشرفته با استانداردهاي خاص ( GMP Lab ) را مرتفع ميكند. اين كار با بالابردن ضريب ايمني كار، احتمال انتقال آلودگي و عفونت به بيمار را منتفي ميسازد.
3- تمام مراحل تهية نمونه مغز استخوان، جداسازي سلولها و پيوند آنها، در اتاق عمل و صرفاً توسط خود جراح قلب صورت ميگيرد. بنابراين، با استفاده از اين شيوه نيازي به همكاري گروه ديگري از متخصصان مانند هماتولوژيستها و غيره نيست.
4- با توجه به اينكه در اين روش علاوه بر تزريق سلولهاي بنيادي به اطراف عضلة دچار عارضه، از خاصيت همافزايي نور ليزر نيز استفاده ميشود، در نتيجة التهاب موقت ايجادشدة ناشي از تابش نور ليزر، خونرساني به ناحية ايسكميك و تزريقشده، افزايش مييابد و با اين كار، احتمال موفقيت در پيوند سلولهاي بنيادي و زنده ماندن سلولهاي پيوندي افزايش مييابد.
اين روش پيوند براي كدام گروه از بيماران قلبي مناسب است؟
شايان ذكر است كه در بيش از 50 درصد بيماران قلبي، قبل از اقدام به عمل جراحي معيارهاي لازم براي پيوند سلولهاي بنيادي وجود دارد. اما با اين روش، در مورد بيماران ديگري كه در حالت اورژانس به بيمارستان منتقل شده و اين تشخيص قبلاً براي آنها داده نشده باشد، ميتوان پس از اقدام به عمل جراحي و در حين كار چنين تصميمي را اتخاذ كرد. براي مثال، اگر بيماراني كه در مرحلة نهايي نارسايي قلبي ( End stage heart failure ) قرار داشته و به علت سختشدن ديواره عروق كرونري، رگهاي درگير بهطور كامل بستهشده و به موقع تحت درمان بايپس قرار نگيرند، جراح تنها پس از باز كردن قفسة سينه بيمار متوجه عدم كارايي روش بايپس براي درمان فرد ميشود. در چنين موارد اورژانسي، ميتوان با پيوند سريع سلولهاي بنيادي به قلب بيمار، جان او را نجات داد.
هزينه پيوند سلولهاي بنيادي با روش مذكور
خصوصيات سلولهاي بنيادي مورد استفاده
جداسازي سلولهاي ACC133 + با استفاده از نانوتكنولوژي
لازم به ذكر است كه در داخل نمونة اخذشدة مغز استخوان، كمتر از 5/1 درصد سلولها از نوع ACC133 + هستند و بقيه شامل ردههاي ديگر سلولي هستند. براي مثال، كمتر از 10 درصد سلولها از نوع CD34 + و حدود 25-20 درصد سلولها CD117 + هستند.
7)كاربردهاي سلولهاي بنيادي در پزشكي
توليد اينترفرونها در زمان خود، انقلاب در پزشكي محسوب شد و اين اميدواري را پيش آورد كه بتواند بهعنوان درمان قطعي سرطان مورد استفاده قرار گيرد؛ اما گذشت زمان برخي محدوديتهاي آن را نمايان ساخت.
پس از آن، ژندرماني به عنوان راهي براي درمان سرطان مطرح شد كه سر و صداي زيادي در مجامع علمي و پزشكي به راه انداخت؛ در اين تكنولوژي، معمولاً از ويروسها به عنوان ناقلين ژنها استفاده ميشود كه مشكلاتي همچون تومورزايي، بيماريزايي و غيره را به همراه دارد و لذا اين روش نيز با محدوديتهاي جدي روبرو شد.
امروزه يكي از كاربردهاي سلولهاي بنيادي كه توجه زيادي را به خود معطوف داشته است، همين درمان سرطان است؛ چرا كه از سلولهاي بنيادي انساني و معمولاً بدون تغيير ژنتيكي، ميتوان براي ترميم بافتهاي آسيب ديده استفاده كرد.
هر چند استفاده از سلولهاي بنيادي، در مراحل اوليه خود به سر ميبرد، اما متخصصين معتقدند در آيندهاي نهچندان دور، كاربردهاي وسيعي در علم پزشكي خواهد داشت. با اين اعتقاد، هماكنون در اقصي نقاط جهان تحقيقات وسيعي در خصوص استفاده از سلولهاي بنيادي در جهت تأمين سلامت انسان در حال انجام است. در ذيل به چند نمونه از كاربردهاي نزديك به حصول سلولهاي بنيادي اشاره ميشود:
1- ترميم بافتهاي آسيبديده قلب
امروزه شمار زيادي از مردم دنيا از بيماريهاي قلبي ناشي از آ?سيبديدگي بافتهاي آن رنج ميبرند كه بعضاً منجر به مرگ نيز ميشود. ترميم بافتهاي آسيبديده، همواره يكي از دغدغههاي پزشكان و متخصصين علوم پزشكي بوده و بهرهگيري از سلولهاي بنيادي، اميد تازهاي در اين عرصه به وجود آورده است. متخصصين اميدوارند سلولهاي بنيادي را از مغز استخوان افراد بيمار (يا جنين نوظهور) استخراج و آنها را در محيط آزمايشگاه به سلولهاي قلبي تبديل نمايند و نهايتاً با تزريق اين سلولهاي تمايزيافته به بدن، امكان ترميم بافتهاي آسيبديده قلب را فراهم آورند.
البته اين تكنيك هنوز در مرحله آزمايشگاهي است، اما موفقيتهاي بهدست آمده در حيوانات آزمايشگاهي، احتمال بهرهگيري از آن را در انسان قوت بخشيده است.
2- ترميم بافتهاي استخواني
در افرادي كه شكستگي وسيع استخوان دارند و يا كساني كه مورد عمل جراحي مغزي قرار گرفته و كاسه سر آنها برداشته شده و همچنين اشخاصي كه استخوانهاي آنها بهكندي جوش ميخورد، از سلولهاي بنيادي براي جوشخوردگي سريع و جلوگيري از عفونتهاي بعدي استفاده ميشود. در اين تكنيك، سلولهاي بنيادي مزانشيمي از فرد گرفته شده و در محيط آزمايشگاه به سلولهاي استئوپلاست (استخواني) تبديل ميشوند، سپس اين سلولها در كنار بافتهاي آسيبديده استقرار مييابند تا باعث جوشخوردگي سريع اين بافتها گردند. در اين مورد، سلولها از خود شخص جدا ميشوند؛ بنابراين مشكل پسزدگي و عوارض جانبي را نيز در برندارد.
تكنيك مذكور از مرحله آزمايشگاهي خارج شده و هماكنون دركشورهاي پيشرفته دنيا از جمله آمريكا و ژاپن به طور عملي و كاربردي بر روي بيماران انجام ميشود.
3- درمان بيماريها و ضايعات عصبي
پيشرفتهاي بشر در زمينه توليد، تكثير و تمايز سلولهاي بنيادي، اين اميد را به وجود آورده است كه بتوان از اين سلولها در مداواي ضايعات عصبي مانند قطع نخاع و بيماريهاي عصبي همچون آلزايمر، پاركينسون، MS و غيره نيز بهره برد. در اين مورد نيز پس از تهيه سلولهاي بنيادي از شخص موردنظر، آنها را به سلول عصبي تبديل نموده و براي ترميم يا مداوا مورد استفاده قرار ميدهند. البته بخش اعظم اين تكنولوژي، در مرحله آزمايشگاهي است؛ اما با پيشرفتهاي خوبي همراه بوده است. بهعنوان مثال، طي گزارشي كه اخيراً منتشره شده، متخصصين فرانسوي موفق شدند با استفاده از سلولهاي مزانشيمي، موش قطع نخاع شدهاي را تا حدي بهبود بخشند كه قادر به حركت باشد ( البته نه با تعادل صددرصد). اين موضوع در صورتيكه با موفقيت نهايي توأم شود، انقلاب بزرگي در پزشكي به شمار ميرود.
ضمن اينكه يك شركت آمريكايي بنام اورسي كه يك مركز تحقيقاتي خصوصي بوده و متخصصين ارشد جهان در زمينه سلولهاي بنيادي را گرد هم آورده، ادعا كرده است كه قادر به مداواي بيماريهايي مانند آلزايمر، پاركينسون، MS و غيره ميباشد كه اين عمل را با استفاده از سلولهاي بنيادي خود شخص انجام ميدهد؛ البته در قبال آن هزينههاي بالايي تا حد 100 هزار دلار دريافت مينمايند.
4- ترميم سوختگيها و ضايعات پوستي
جراحات پوستي ناشي از سوختگي يا صدمات ديگر، بسياري از بيماران را به خود مبتلا نموده است. در روش معمول براي ترميم قسمتهاي صدمهديده، از پوست بخشهاي سالم بدن استفاده ميشود كه مشكلاتي را براي بيمار بهوجود ميآورد. اما با .استفاده از سلولهاي بنيادي ميتوان سلولهاي پوستي را در محيط آزمايشگاه توليد نمود و درترميم بافتهاي صدمهديده از آنها استفاده كرد. اين تكنولوژي در حال حاضر، كاربردي شده و توسط يكي از بيمارستانهاي انگلستان مورد استفاده قرار ميگيرد.
5- ترميم لوزالمعده (پانكراس) و ترشح انسولين
اخيراً در دانشگاه آلبرتا كانادا، متخصصين موفق شدند سلولهاي بنيادي مزانشيمي را به سلولهاي پانكراس انساني تبديل نمايند و به بيماران ديابتي منتقل نمايند. اين آزمايش بر روي 23 نفر انجام شد كه 16 نفر از تزريق انسولين بينياز شدند. يادآوري ميشود كه اين پيوند از نوع اتولوگ بود (براي مداواي هر شخص از سلولهاي بنيادي خود وي استفاده شد) و مشكلات جانبي در بر نداشت.
6- آزمون تأثير داروهاي جديد
داروهاي سنتتيك جديد ممكن است بر سلولها يا بافتهاي انساني تأثيرات متفاوتي داشته باشند كه امكان تست آنها در انسانها به دليل مسايل اخلاق پزشكي وجود ندارد. بهعنوان مثال، يك داروي سنتتيك قلبي ممكن است بر سلولها يا بافتهاي قلبي تأثير سويي داشته باشد. در اين موارد ميتوان سلولهاي قلبي يا هر بافت ديگر را با استفاده از سلولهاي بنيادي توليد نمود و داروهاي جديد را بر روي آنها آزمايش كرد، بدون اينكه نياز به آزمايش در بدن انسان باشد (آزمايشات مقدماتي انساني). در اين خصوص سلولهاي بنيادي جنيني ميتوانند كاربرد وسيعي داشته باشند.
7- ترميم ساير بافتهاي آسيبديده
مواردي كه اشاره شد كاربردهايي از سلولهاي بنيادي بود كه به صورت كاربردي درآمده بودند و يا نزديك به كاربردي شدن هستند، اما از كاربردهاي بالقوه اين سلولها ميتوان به ترميم بافتهاي آسيب ديده ديگر بدن از جمله غضروف، كبد، ماهيچه و غيره اشاره كرد كه ميتواند دامنه كاربرد سلولهاي بنيادي را در آينده افزايش دهد.
يك نكته مهم
در اطلاعرساني عمومي كاربرد سلولهاي بنيادي، بايد به اين نكته توجه شود كه انتظارات بيش از حد توانايي اين تكنولوژي در مردم به وجود نيايد. ساخت اندام، يكي از اميدهايي است كه ممكن است در برخي از مردم ايجاد گردد؛ بايد خاطر نشان كرد. كه با دانش كنوني بشر، امكان توليد عضو يا اندام توسط اين تكنولوژي وجود ندارد و به نظر نميرسد در آيندهاي نزديك نيز اين امر محقق شود. بهعنوان مثال، اگر قلب را در نظر بگيريم علاوه بر شكل آن كه در كاركردش بسيار حايز اهميت است، از سلولها و بافتهاي مختلفي از جمله بافت ماهيچهاي، خوني، اپيدرمي، رگ و غيره درست شده است. اگر بخواهيم سلولهاي بنيادي را به هر يك از اين بافتها تبديل نماييم، نيازمند اعمال شرايط و تيمارهاي ويژهاي هستيم كه فراهم كردن همه آنها به طور همزمان در يك بيورآكتور غيرممكن است. شايد در آينده بشر بتواند اين اعضاء را دربدن انسان يا حيوان توليد نمايد كه بهويژه در مورد دوم علاوه بر مشكلات تكنيكي با محدوديتهاي اخلاقي نيز مواجه است.
با اين تفاسير، كاربرد قابل انتظار بهرهگيري از سلولهاي بنيادي در شرايط فعلي و آينده نزديك، ترميم بافتهاي آسيبديده است كه در موارد فوق به آنها اشاره شد. هر چند همين كاربردها نيز در صورت فراگيرشدن، انقلابي در پزشكي محسوب ميشوند.
منابع:
همشهری امارات
خبرگزارى فارس
http://www.salamatiran.com
http://www.hamshahrionline.ir
http://www.irshafa.ir
http://bio.itan.ir
http://www.jazirehdanesh.com
http://www.bazyab.ir