نویسندگان: مارگارت. آ. نولز
پیتر. جی. سلبی
مترجم: حبیب الله علیخانی
پیتر. جی. سلبی
مترجم: حبیب الله علیخانی
چگونه تومورها وجود دارند: برخی اثرات تومورها بر روی بدن
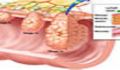
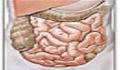
تومورها معمولاً در زمانی شناسایی می شوند که آنها اثراتی ایجاد کنند. تومورهای پوستی یا اندام هایی که به سهولت مورد بررسی قرار می گیرند مانند پستان، اغلب به صورت توده ی قابل تشخیص می باشند. بسیاری از سلول ها در تومورها می میرند و این سلول های مرده موجب رهایش آنزیم هایی می شود که موجب تخریب بافت های زیرین می شود. در این حالت، زخم غیر قابل ترمیم ایجاد می شود. رگ های خونی در زیر زخم تخریب می شوند به نحوی که خون ریزی رخ می دهد. در روده و یا سستم ادراری، خون ممکن است در ادرار و یا مدفوع یافت شوند به نحوی که خون ریزی در یک علامت در این اندام ها می باشد. بسیاری از این اثرات که بوسیله ی تومورها ایجاد می شود، به دلیل موقعیت توموری است که ممکن است تحت فشار قرار گیرد و یا بافت اطراف خود را تخریب کند. این تومورها همچنین می تواند منجر به تحت فشار قرار گرفتن عصب و یا ایجاد درد شود. برای مثال، تومورهای موجود در روده ممکن است موجب انسداد روده شوند زیرا توده ی توموری در حفره ی روده رشد می کند و یا رشد دیواره و تخریب ماهیچه ها، را در پی داشته باشد. تومورهای مغزی ممکن است موجب بروز سر درد شوند. این مسئله به دلیل ایجاد فشار در داخل جمجمه ایجاد می شود. تومورها مجرای صفراوی را درگیر کرده و این مسئله منجر به زردی می شود. اثرات فیزیکی به صورت واضح به مکان دقیق تومور، وابسته می باشد. برخی تومورها مخصوصاً آنهایی که در اندام های تولید کننده ی هورمون ایجاد می شوند، ممکن است اثراتی بر روی تولید هورمون داشته باشند. در برخی موارد نیز، اثربخشی هورمون ها بوسیله ی تخریب سلول های غدد طبیعی، کاهش می یابد. در برخی موارد ندرت نیز این بخش ها موجب تولید هورمون های غیر متعارفی می شوند که ممکن است موجب اثرات قابل توجهی بر بدن شود. برای مثال، برخی از تومورهای ریه ای ممکن است هورمون هایی تولید کنند که به صورت نرمال بوسیله ی غدد هیپوفیز تولید می شوند. کم خونی به دلیل خون ریزی از تومورها و یا به دلیل برخی اثرات سمی بر روی مغز استخوان ایجاد می شود. این موارد به عنوان علائم متداول در بیشتر سلول ها می باشد. مشابه این اثرات، بسیاری از تومورها ممکن است اشتها را کاهش دهند و برخی اوقات حتی تومورهای اولیه هنوز هم کوچک می باشند. عوامل ایجاد کننده شناخته شده نیست اما برخی اوقات علت این مسئله تولید مواد سمی بوسیله ی تومور می باشد (مثلا فاکتور رشد).
به هر حال، ما تنها در مراحل اولیه از کاربد این روش های جدید هستیم. در بسیاری موارد، درمان ممکن است ممکن نباشد زیرا تومورها اندام های حیاتی بدن را درگیر کرده و یا به طور گسترده ای در بدن گسترش یافته اند. اگر چه از لحاظ تئوری، این مسئله نامطلوب است، گسترش تومور از مراحل اولیه ی بیماری، اتفاق می افتد و از این رو، جراحی محلی و درآوردن تومور اولیه، امروزه نیز یکی از مؤثرترین روش های درمان در برخی موارد است. چاقوی کوچک جراحی هنوز هم بهترین سلاح برای مباره است اما تلاش ها به منظور بهبود روش های جراحی با استفاده از انرژی لیزر و یا جراحی سرمایی با استفاده از پروب های نیتروژن مایع نیز در حال انجام می باشد. یک روش تجربی استفاده از داروهای حساس به نور می باشد که ممکن است در تومور متمرکز شوند و به صورت محلی و با استفاده از انرژی لیزر فعال سازی شوند. درمان با تابش نیز یکی دیگر از روش های متداول مورد استفاده برای تخریب تومورها می باشد اما این روش اغلب مشکلاتی را ایجاد می کند. برخی از سلول های توموری همچنین در برابر تخریب با تابش، مقاوم هستند. هم اکنون، در روش های جدید، تابش با عوامل دیگر از جمله عوامل حساس کننده نسبت به تابش، ترکیب شده است. شیمی درمانی نیز یکی از روش های اصلی برای درمان بیماری سرطان منتشر شده می باشد. برخی از روش های درمان منفرد و یا چند عاملی نیز هنوز مورد استفاده قرار می گیرند اما پیشرفت های اخیر در زمینه ی بهینه سازی استفاده از عوامل قدیمی و معرفی عوامل جدید مانند مولکول های کوچک هدفمند، نیز در حال انجام می باشد. سایر عوامل جدید مانند مولکول های بیولوژیکی مانند آنتی بادی ها و اصلاح کننده های پاسخ بیولوژیکی مانند سیتوکین ها نیز در حال بررسی می باشند. به طور مشابه، پیشرفت های بزرگی در زمینه ی قابلیت ما برای مهار سیستم ایمنی میزبان نیز انعکاس دهنده ی روش های جدیدی است که ایمنوتراپی نامیده می شوند.
نه تنها در روش های جدید از مارکرهای خاص سرطان به عنوان اهداف برای طراحی دارو، استفاده می شود، بلکه همچنین دانستن در مورد تغییرات مولکولی در سلول های سرطانی نیز اطلاعات ارزشمندی ارائه کرده است که بدین وسیله، می توان روش های درمانی ژنی نیز توسعه پیدا کند. بسیاری از روش ها مورد بررسی قرار گرفته اند. در این روش ها، تلاش شده است تا عملکرد ژنی مؤثر را جایگزین کنیم (ممانعت کننده های رشد توموری مانند ژن های مختلف از جمله p53, Rb). با این کار، می توان پروداروها و یا سایر مولکول های درمانی خوبی به منظور درمان هدفمند تولید کرد. عقل سلیم پیشنهاد می دهد که درمان اولیه باید منجر به نتایج پایانی بهتری شود و به همین دلیل، برنامه های غربال گری گستره و گران قیمتی برای پیدا کردن و شناسایی تومورها پیش از عود بیماری در حال انجام می باشد. غربال گری برای بررسی وجود سرطان برای سرطان هایی مانند سرطان رحم، پستان، روده، تخمدان، پروستات و در برخی مناطق، سرطان معده (ژاپن و چین) و کبد (آفریقای جنوبی) انجام شده است. دو مشکل اصلی در مورد این اشکال درمانی، تنوع عوامل درمانی، سلول های توموری انتشار یافته و مشخصه ی هر یک از این تومورها می باشد. این مسئله تنها موجب محدود شدن اثرات سمیت برای سلول های توموری می شود، بدون آنکه موجب تخریب بافت نرمال شود. تشخیص مارکرهای خاص تومورها، اجازه ی توسعه ی آنتی بادی های ضد تومور خاص را می دهد. برخی از مولکول های خاص تومور در چند سال اخیر شناسایی شده اند و از آنها برای توسعه ی روش های درمانی استفاده شده است. ولو اینکه مارکرهای مطلق برای تمام تومورها موجود نباشد، این مسئله هنوز ممکن است که از آنتی بادی ها در برابر بافت های نرمال استفاده شود اگر، عوامل تعیین کننده ی خاص بافت در جایی قرار گرفته باشند که معماری بافت در تومور توزیع شده باشد. تحقیقات بیولوژی مولکولی هم اکنون تلاش زیادی در این زمینه انجام داده است.
جلوگیری در واقع بر اساس اجتناب از عوامل سرطان زا انجام می شود. از آنجایی که سرطان ریه به صورت منفرد مسئول مرگ و میر یک چهارم از مرگ و میرهای ناشی از سرطان است، جلوگیری از مصرف سیگار و سایر مواد مرتبط با تنباکو، در حقیقت می تواند موجب کاهش قابل توجهی در ایجاد سرطان شود. کاهش سایر عوامل محیطی خطرناک و اثر نوع وعده ی غذایی نیز نقش کمتری دارند و تشخیص اثر نوع غذای مصرفی بر روی سرطان هنوز واضح نیست.
عقل سلیم پیشنهاد می دهد که درمان اولیه باید منجر به نتایج پایانی بهتری شود و به همین دلیل، برنامه های غربال گری گستره و گران قیمتی برای پیدا کردن و شناسایی تومورها پیش از عود بیماری در حال انجام می باشد. غربال گری برای بررسی وجود سرطان برای سرطان هایی مانند سرطان رحم، پستان، روده، تخمدان، پروستات و در برخی مناطق، سرطان معده (ژاپن و چین) و کبد (آفریقای جنوبی) انجام شده است. به صورت ایده آل، غربال گری باید موجب کاهش میزان مرگ و میر و عوامل جانبی سرطان شود و برای برهی از سرطان ها، این اعتقاد وجود دارد که غربال گری مزیت دارد (مثلا سرطان پستان و تخمدان). به هر حال، مزیت های هنوز واضح نیست. برای مثال، برخی ادعا کرده اند که غربال گری ممکن است تومورهای کوچک را تشخیص دهد که هیچگاه عامل عود بیماری نمی شوند. سرطان می تواند در پروستات حدود 30 تا 40 % از مردانی مشاهده شود که به بیماری های غیر سرطانی مبتلا هستند. از آنجایی که این 30 تا 40 % از مردان از سرطان پرستان نمی میرند، این اعتقاد وجود دارد که بیشتر این تومورها، موجب کشته شدن میزبان نمی شود. تومورهای مشابه پنهان می توانند در بسیاری از اندام دیگر مشاهده شند، اگر چه فراوانی آنها به میزان تومورهای پروستات، نیست.
اگر چه بیشتر بیشتر این اطلاعات از تکنولوژی های کنونی و همچنین داده های مربوط به آزمایشگاه های پاتولوژی بدست آمده است، یک چنین مطالعه هایی به صورت قابل توجهی مشاهداتی است و دستکاری های تجربی گسترده در انسان، مقدور نمی باشد. بنابراین، توسعه ی روش هایی که اجازه ی دستکاری تجربی سلول ها و تومورها را می دهد و همچنین موجب افزایش گستره ی تشخیص مولکول ها می شود، نیز مورد نیاز می باشد. یک گستره وسیع از روش ها هم اکنون موجود می باشد. این روش ها می توانند هیجان آور و دلهره برانگیز باشند. یک بررسی جزئی در مورد چیزی که موجود می باشد، در حقیقت باید حاوی جوانب مربوط به علم بالینی، بیولوژی، فیزیک و شیمی باشد.
سوال های بی پاسخ در مورد تحقیقات سرطان امروزه نیازمند یک سری مهارت های بیولوژیکی و بالینی می باشد. برای مثال، بررسی نمونه های توموری با استفاده از میکروآرایه های مربوط به عوامل خاص که در حقیقت موجب بروز چالش های آزمایشگاهی و بیواینفورماتیک می شود، ممکن است منجر به رشد سریع بررسی یک گستره از عوامل ژنی کاندید شود. این عوامل برای ایزولاسیون توالی های ژنی، افزایش میزان یک عامل شیمیایی، افزایش در میزان آنتی بادی ها، محیط سلولی، مدولاسیون میزان ژن و ...، مورد نیاز می باشند. این تصور وجود دارد که تمام این فعالیت ها بوسیله ی محققین منفرد انجام می شود و آنها به طور متداول بوسیله ی تیم های تحقیقاتی مجزا و آزمایشگاه های آنها انجام می شود. در حقیقت، چیزی که در اینجا، خودنمایی می کند، در واقع مشارکت و ارتباطی است که در واقع می تواند مهارت ها و ابزارهای تحقیقات سرطان را گسترش دهد.
استفاده از مطالب این مقاله، با ذکر منبع راسخون، بلامانع می باشد. منبع مقاله :
Introduction to the Cellular and Molecular Biology of Cancer/ Margaret A. Knowles and Peter J. Selby
تومورها معمولاً در زمانی شناسایی می شوند که آنها اثراتی ایجاد کنند. تومورهای پوستی یا اندام هایی که به سهولت مورد بررسی قرار می گیرند مانند پستان، اغلب به صورت توده ی قابل تشخیص می باشند. بسیاری از سلول ها در تومورها می میرند و این سلول های مرده موجب رهایش آنزیم هایی می شود که موجب تخریب بافت های زیرین می شود. در این حالت، زخم غیر قابل ترمیم ایجاد می شود. رگ های خونی در زیر زخم تخریب می شوند به نحوی که خون ریزی رخ می دهد. در روده و یا سستم ادراری، خون ممکن است در ادرار و یا مدفوع یافت شوند به نحوی که خون ریزی در یک علامت در این اندام ها می باشد. بسیاری از این اثرات که بوسیله ی تومورها ایجاد می شود، به دلیل موقعیت توموری است که ممکن است تحت فشار قرار گیرد و یا بافت اطراف خود را تخریب کند. این تومورها همچنین می تواند منجر به تحت فشار قرار گرفتن عصب و یا ایجاد درد شود. برای مثال، تومورهای موجود در روده ممکن است موجب انسداد روده شوند زیرا توده ی توموری در حفره ی روده رشد می کند و یا رشد دیواره و تخریب ماهیچه ها، را در پی داشته باشد. تومورهای مغزی ممکن است موجب بروز سر درد شوند. این مسئله به دلیل ایجاد فشار در داخل جمجمه ایجاد می شود. تومورها مجرای صفراوی را درگیر کرده و این مسئله منجر به زردی می شود. اثرات فیزیکی به صورت واضح به مکان دقیق تومور، وابسته می باشد. برخی تومورها مخصوصاً آنهایی که در اندام های تولید کننده ی هورمون ایجاد می شوند، ممکن است اثراتی بر روی تولید هورمون داشته باشند. در برخی موارد نیز، اثربخشی هورمون ها بوسیله ی تخریب سلول های غدد طبیعی، کاهش می یابد. در برخی موارد ندرت نیز این بخش ها موجب تولید هورمون های غیر متعارفی می شوند که ممکن است موجب اثرات قابل توجهی بر بدن شود. برای مثال، برخی از تومورهای ریه ای ممکن است هورمون هایی تولید کنند که به صورت نرمال بوسیله ی غدد هیپوفیز تولید می شوند. کم خونی به دلیل خون ریزی از تومورها و یا به دلیل برخی اثرات سمی بر روی مغز استخوان ایجاد می شود. این موارد به عنوان علائم متداول در بیشتر سلول ها می باشد. مشابه این اثرات، بسیاری از تومورها ممکن است اشتها را کاهش دهند و برخی اوقات حتی تومورهای اولیه هنوز هم کوچک می باشند. عوامل ایجاد کننده شناخته شده نیست اما برخی اوقات علت این مسئله تولید مواد سمی بوسیله ی تومور می باشد (مثلا فاکتور رشد).
چگونه سرطان کشنده می شود؟
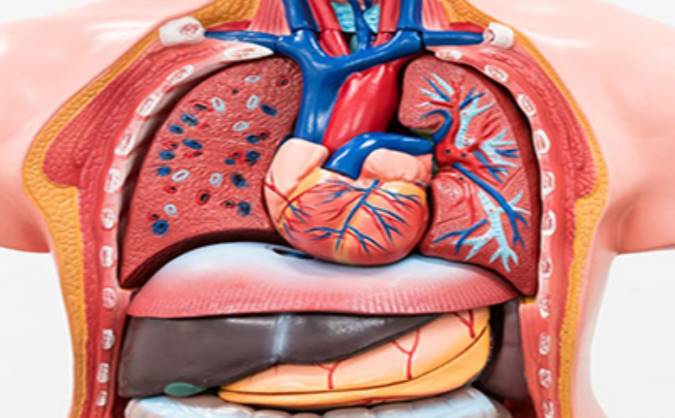
همانگونه که مشاهده می شود، بسیاری از سرطان ها در افراد پیر ایجاد می شوند و یک تعداد زیاد از بیماران به دلیل این بیماری نمی میرند اما برخی از شرایط غیر مرتبط مانند بیماری قلب یا عفونت های عارض شده در این بین، منجر به فوت می شود. هدف از درمان سرطان، حذف و یا تخریب تمام سلول های سرطانی و مکان هایی که مستعد توسعه ی سرطان هستند. هم اکنون درمان می تواند یک سری روش ها و یا تکنیک ها باشد که در حقیقت بر اساس درمان های استاندارد می باشند (مانند درمان با جراحی، پرتودرمانی و یا شیمی درمانی). برخی از درمان ها نیز شامل استفاده از عوامل بیولوژیکی، ایمنوتراپی و استفاده از مولکول های ویژه و جدید می باشد. رویدادهای مرتبط با تومور ممکن است موجب مرگ مستقیم و یا غیر مستقیم شود. این مسئله به مکان قرارگیری تومور و میزان گسترش تومور، ربط دارد. یک عامل متداول در مرگ، درگیری شدن اندام های حیاتی بدن (به دلیل تهاجم مستقیم محلی و یا ایجاد متاستاز) می باشد برای مثال، در مغز، ریه یا کبد. به ندرت، مرگ ممکن است به دلیل خونریزی ایجاد شود. در اغلب موارد، کم خونی و ضایعات غیر قابل پیش بینی ممکن است منجر به کاهش مقاومت در برابر عفونت ها می شود و بدین صورت برونکوپنیومونی پایانی و یا عفونت مجاری ادراری ممکن است بروز کند. در بسیاری موارد، نمی توان علت مرگ را تشخیص داد.درمان سرطان
هدف از درمان سرطان، حذف و یا تخریب تمام سلول های سرطانی و مکان هایی که مستعد توسعه ی سرطان هستند. هم اکنون درمان می تواند یک سری روش ها و یا تکنیک ها باشد که در حقیقت بر اساس درمان های استاندارد می باشند (مانند درمان با جراحی، پرتودرمانی و یا شیمی درمانی). برخی از درمان ها نیز شامل استفاده از عوامل بیولوژیکی، ایمنوتراپی و استفاده از مولکول های ویژه و جدید می باشد. چیزی که واضح است، این است که تکنولوژی های جدید در راه است.به هر حال، ما تنها در مراحل اولیه از کاربد این روش های جدید هستیم. در بسیاری موارد، درمان ممکن است ممکن نباشد زیرا تومورها اندام های حیاتی بدن را درگیر کرده و یا به طور گسترده ای در بدن گسترش یافته اند. اگر چه از لحاظ تئوری، این مسئله نامطلوب است، گسترش تومور از مراحل اولیه ی بیماری، اتفاق می افتد و از این رو، جراحی محلی و درآوردن تومور اولیه، امروزه نیز یکی از مؤثرترین روش های درمان در برخی موارد است. چاقوی کوچک جراحی هنوز هم بهترین سلاح برای مباره است اما تلاش ها به منظور بهبود روش های جراحی با استفاده از انرژی لیزر و یا جراحی سرمایی با استفاده از پروب های نیتروژن مایع نیز در حال انجام می باشد. یک روش تجربی استفاده از داروهای حساس به نور می باشد که ممکن است در تومور متمرکز شوند و به صورت محلی و با استفاده از انرژی لیزر فعال سازی شوند. درمان با تابش نیز یکی دیگر از روش های متداول مورد استفاده برای تخریب تومورها می باشد اما این روش اغلب مشکلاتی را ایجاد می کند. برخی از سلول های توموری همچنین در برابر تخریب با تابش، مقاوم هستند. هم اکنون، در روش های جدید، تابش با عوامل دیگر از جمله عوامل حساس کننده نسبت به تابش، ترکیب شده است. شیمی درمانی نیز یکی از روش های اصلی برای درمان بیماری سرطان منتشر شده می باشد. برخی از روش های درمان منفرد و یا چند عاملی نیز هنوز مورد استفاده قرار می گیرند اما پیشرفت های اخیر در زمینه ی بهینه سازی استفاده از عوامل قدیمی و معرفی عوامل جدید مانند مولکول های کوچک هدفمند، نیز در حال انجام می باشد. سایر عوامل جدید مانند مولکول های بیولوژیکی مانند آنتی بادی ها و اصلاح کننده های پاسخ بیولوژیکی مانند سیتوکین ها نیز در حال بررسی می باشند. به طور مشابه، پیشرفت های بزرگی در زمینه ی قابلیت ما برای مهار سیستم ایمنی میزبان نیز انعکاس دهنده ی روش های جدیدی است که ایمنوتراپی نامیده می شوند.
نه تنها در روش های جدید از مارکرهای خاص سرطان به عنوان اهداف برای طراحی دارو، استفاده می شود، بلکه همچنین دانستن در مورد تغییرات مولکولی در سلول های سرطانی نیز اطلاعات ارزشمندی ارائه کرده است که بدین وسیله، می توان روش های درمانی ژنی نیز توسعه پیدا کند. بسیاری از روش ها مورد بررسی قرار گرفته اند. در این روش ها، تلاش شده است تا عملکرد ژنی مؤثر را جایگزین کنیم (ممانعت کننده های رشد توموری مانند ژن های مختلف از جمله p53, Rb). با این کار، می توان پروداروها و یا سایر مولکول های درمانی خوبی به منظور درمان هدفمند تولید کرد. عقل سلیم پیشنهاد می دهد که درمان اولیه باید منجر به نتایج پایانی بهتری شود و به همین دلیل، برنامه های غربال گری گستره و گران قیمتی برای پیدا کردن و شناسایی تومورها پیش از عود بیماری در حال انجام می باشد. غربال گری برای بررسی وجود سرطان برای سرطان هایی مانند سرطان رحم، پستان، روده، تخمدان، پروستات و در برخی مناطق، سرطان معده (ژاپن و چین) و کبد (آفریقای جنوبی) انجام شده است. دو مشکل اصلی در مورد این اشکال درمانی، تنوع عوامل درمانی، سلول های توموری انتشار یافته و مشخصه ی هر یک از این تومورها می باشد. این مسئله تنها موجب محدود شدن اثرات سمیت برای سلول های توموری می شود، بدون آنکه موجب تخریب بافت نرمال شود. تشخیص مارکرهای خاص تومورها، اجازه ی توسعه ی آنتی بادی های ضد تومور خاص را می دهد. برخی از مولکول های خاص تومور در چند سال اخیر شناسایی شده اند و از آنها برای توسعه ی روش های درمانی استفاده شده است. ولو اینکه مارکرهای مطلق برای تمام تومورها موجود نباشد، این مسئله هنوز ممکن است که از آنتی بادی ها در برابر بافت های نرمال استفاده شود اگر، عوامل تعیین کننده ی خاص بافت در جایی قرار گرفته باشند که معماری بافت در تومور توزیع شده باشد. تحقیقات بیولوژی مولکولی هم اکنون تلاش زیادی در این زمینه انجام داده است.
بیشتر بخوانید:نور درمانیِ سرطان
جلوگیری از سرطان و غربال گری
از آنجایی که حداقل یک نفر از بین 4 نفر در برخی از دوران زندگی خود با سرطان مواجه می شود، جلوگیری از بروز این مسئله در حقیقت می توان یک روش مناسب باشد. به هر حال، 70 % از تمام سرطان هایی در افراد بیش از 60 سال ایجاد می شود و حتی جلوگیری از همه ی این سرطان ها نیز نمی تواند اثر مهمی بر روی عمر مفید انسان داشته باشد. منطق جلوگیری از بروز و درمان مؤثر در حقیقت موجب بهبود کیفیت زندگی می شود.جلوگیری در واقع بر اساس اجتناب از عوامل سرطان زا انجام می شود. از آنجایی که سرطان ریه به صورت منفرد مسئول مرگ و میر یک چهارم از مرگ و میرهای ناشی از سرطان است، جلوگیری از مصرف سیگار و سایر مواد مرتبط با تنباکو، در حقیقت می تواند موجب کاهش قابل توجهی در ایجاد سرطان شود. کاهش سایر عوامل محیطی خطرناک و اثر نوع وعده ی غذایی نیز نقش کمتری دارند و تشخیص اثر نوع غذای مصرفی بر روی سرطان هنوز واضح نیست.
عقل سلیم پیشنهاد می دهد که درمان اولیه باید منجر به نتایج پایانی بهتری شود و به همین دلیل، برنامه های غربال گری گستره و گران قیمتی برای پیدا کردن و شناسایی تومورها پیش از عود بیماری در حال انجام می باشد. غربال گری برای بررسی وجود سرطان برای سرطان هایی مانند سرطان رحم، پستان، روده، تخمدان، پروستات و در برخی مناطق، سرطان معده (ژاپن و چین) و کبد (آفریقای جنوبی) انجام شده است. به صورت ایده آل، غربال گری باید موجب کاهش میزان مرگ و میر و عوامل جانبی سرطان شود و برای برهی از سرطان ها، این اعتقاد وجود دارد که غربال گری مزیت دارد (مثلا سرطان پستان و تخمدان). به هر حال، مزیت های هنوز واضح نیست. برای مثال، برخی ادعا کرده اند که غربال گری ممکن است تومورهای کوچک را تشخیص دهد که هیچگاه عامل عود بیماری نمی شوند. سرطان می تواند در پروستات حدود 30 تا 40 % از مردانی مشاهده شود که به بیماری های غیر سرطانی مبتلا هستند. از آنجایی که این 30 تا 40 % از مردان از سرطان پرستان نمی میرند، این اعتقاد وجود دارد که بیشتر این تومورها، موجب کشته شدن میزبان نمی شود. تومورهای مشابه پنهان می توانند در بسیاری از اندام دیگر مشاهده شند، اگر چه فراوانی آنها به میزان تومورهای پروستات، نیست.
بیشتر بخوانید:مراحل پیشرفت سرطان
روش های تجربی در تحقیقات سرطان
بیشتر دانش ما در مورد توسعه و رشد تومورها، از مطالعه ی سرطان در بیماران انجام شده است. این مطالعه ها، به صورت بالینی و پاتولوژیکی صورت می گیرد.اگر چه بیشتر بیشتر این اطلاعات از تکنولوژی های کنونی و همچنین داده های مربوط به آزمایشگاه های پاتولوژی بدست آمده است، یک چنین مطالعه هایی به صورت قابل توجهی مشاهداتی است و دستکاری های تجربی گسترده در انسان، مقدور نمی باشد. بنابراین، توسعه ی روش هایی که اجازه ی دستکاری تجربی سلول ها و تومورها را می دهد و همچنین موجب افزایش گستره ی تشخیص مولکول ها می شود، نیز مورد نیاز می باشد. یک گستره وسیع از روش ها هم اکنون موجود می باشد. این روش ها می توانند هیجان آور و دلهره برانگیز باشند. یک بررسی جزئی در مورد چیزی که موجود می باشد، در حقیقت باید حاوی جوانب مربوط به علم بالینی، بیولوژی، فیزیک و شیمی باشد.
سوال های بی پاسخ در مورد تحقیقات سرطان امروزه نیازمند یک سری مهارت های بیولوژیکی و بالینی می باشد. برای مثال، بررسی نمونه های توموری با استفاده از میکروآرایه های مربوط به عوامل خاص که در حقیقت موجب بروز چالش های آزمایشگاهی و بیواینفورماتیک می شود، ممکن است منجر به رشد سریع بررسی یک گستره از عوامل ژنی کاندید شود. این عوامل برای ایزولاسیون توالی های ژنی، افزایش میزان یک عامل شیمیایی، افزایش در میزان آنتی بادی ها، محیط سلولی، مدولاسیون میزان ژن و ...، مورد نیاز می باشند. این تصور وجود دارد که تمام این فعالیت ها بوسیله ی محققین منفرد انجام می شود و آنها به طور متداول بوسیله ی تیم های تحقیقاتی مجزا و آزمایشگاه های آنها انجام می شود. در حقیقت، چیزی که در اینجا، خودنمایی می کند، در واقع مشارکت و ارتباطی است که در واقع می تواند مهارت ها و ابزارهای تحقیقات سرطان را گسترش دهد.
نتیجه گیری
سرطان یک بیماری پیچیده است و این به نظر می رسد که اگر چه بسیاری از فرایندهای مولکولی متضمن امروزه از یک راز به تکنولوژی تبدیل شده اند، هنوز هم سوالات بی پاسخی برای آینده یافت می شود.استفاده از مطالب این مقاله، با ذکر منبع راسخون، بلامانع می باشد. منبع مقاله :
Introduction to the Cellular and Molecular Biology of Cancer/ Margaret A. Knowles and Peter J. Selby