مترجم: حبیب الله علیخانی
منبع:راسخون
منبع:راسخون
ویروس های توموری موجب ایجاد تغییرات چندگانه در فنوتیپ سلولی می شوند
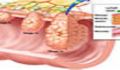
مشابه با سلول های تغییر شکل یافته ی RSV، سلول هایی که بوسیله ی SV40 تغییر شکل یافته اند، دارای شکل تغیری یافته ای هستند و بر روی هم تجمع می یابند. این فقدان در ایجاد ممانعت تماسی، تنها یکی از چند تغییری است که در سلول های تغییر شکل یافته بوسیله ی ویروس، ایجاد می شود. در واقع، سلول های نرمال در محیط رشد، تکثیر نخواهند کرد، مگر آنکه آنها فاکتورهای شروع کننده ی رشد را دریافت کنند. سلول هایی که بوسیله ی یک تعداد از ویروس های توموری مختلف، تغییر شکل می یابند، نیازی به این فاکتورها برای رشد ندارند.وقتی سلول های تغییر شکل یافته، در ژل آگار قرار داده می شود، این سلول ها، قادرند تا رشد کرده و به صورت کلونی های کروی حاوی صد یا هزاران سلول می باشد (شکل 1). این قابلیت تکثیر بدون چسبیدن به زیرلایه ی جامد، موجب می شود تا کف پتری به حالت خاصی در آید. برخلاف آن، سلول های نرمال، نیازمند اتصال به زیرلایه را پیش از رشد دارند و بنابراین، وابسته به زیرلایه می باشند. این قابلیت سلول سلول بدون اتصال به زیرلایه، معمولاً به عنوان شاخص خوبی برای بررسی قابلیت آنها به تشکیل تومور در بدن، تلقی می شود.
اغلب، این ممکن است که میزان تومورزایی ویروس توموری را در سلول های آلوده شده ی یک حیوان میزبان ، بررسی کرد. علت این مسئله ساده است، در واقع، سلول های مورد مطالعه، از یک گونه بوجود آمده اند که میزبان های ژنتیکی غریزی، در این حالت، وجود ندارد. این مسئله استفاده از میزبان های دارای نقص ایمنی را در حالتی اجباری می کند که سیستم ایمنی شان، می تواند در برابر انواع مختلفی از سلول های خارجی، مقاومت کنند. موش با نژاد نودی (Nude strain) به زودی به مهم ترین میزبان مورد استفاده در آزمون تومورزایی تبدیل شد. در اغلب موارد، سلول های توموری، به صورت زیر جلدی تزریق می شوند و مستقیم وارد پوست این حیوان می شوند. از آنجایی که این نژاد از موش، مو ندارد، موش نودی مزیت های بالقوه ای نسبت به سایر موش ها دارد (شکل 2).
ژنوم های ویروس توموری بوسیله ی ایجاد بخشی از DNA سلول میزبان، در سلول تغیییر شکل یافته، مقاومت می کنند
تجربیات برکلی شواهدی مهم در مورد این مسئله مهیا کرده است که اعمال پیوسته ی ژنوم RSV نیازمند حفظ حالت تغییر شکل یافته ی سلول ها می باشد.
این بدین معناست که برخی یا تمام اطلاعات ژنتیکی ویروس، نیازمند همبستگی در برخی اشکال می باشد و از سلول والد به سلول منتج شده، انتقال می یابند. به طور عکس، یک خطا در انتقال این ژن های ویروسی به سلول های ایجاد شده، منجر به تغییر در رفتار نرمال سلول ها، می شود.
به موازات رفتار RSV، تغییر سلولی بوسیله ی دو ویروس توموری DNA ایجاد می شود. این دو ویروس، عبارتند از ویروس SV40 و ویروس پولیما. این به نظر می رسد که این دو ویروس، به حضور پیوسته ی ژنوم های ویروسی در سلول نسل بعدی منتج شده از یک سلول تغییر شکل یافته، وابسته است. این شواهد از کشف پروتئین های توموری دخیل (آنتی ژن های T) در سرطان های ایجاد شده بوسیله ی این دو ویروس، بدست آمده است. برای مثال، سرم تهیه شده از موش حامل یک تومور ایجاد شده از SV40، نشاندهنده ی فعالیت بالای یک پروتئین موجود در هسته ی سلول می باشد که در تومورهای ایجاد شده بوسیله ی Sv40 یافت می شوند. این پروتئین در تومورهای ایجاد شده بوسیله ی ویروس پلی یوما یا سایر تومورهای سرطانی، مشاهده نشده اند. مفهوم این مسئله، این است که ژنوم ویروسی موجود در این سلول های توموری، پروتئینی ایجاد می کنند که موجب پاسخ های ایمنی شدید در موش های مبتلا به تومور می شود (شکل 3).
انتقال سلول به سلول ژنوم های ویروسی در طی نسل های سلولی متوالی، بیان کننده ی یک مسئله مفهومی کلی است. ژن های سلولی، به طور واضح از سلول های والد به سلول های نسل بعدی، انتقال می یابداین کار از طریق فرایندهای برنامه ریزی شده ی دقیق مربوط به تکثیر DNA کروموزومی، و میتوزی انجام می شود که در طی هر سیکل رشد و تقسیم سلولی، مشاهده می شوند. چگونه ژنوم های ویروسی می توانند به طور موفقیت آمیز تکثیر شوند و به طور مؤثر در طی نسل های متوالی، انتقال یابند؟ این مسئله یک مورد پیچیده است زیرا این به نظر می رسد که ژنوم های ویروسی، از فقدان المان های ژنتیکی، رنج می برد.
علاوه بر این، با این حقیقت مواجه هستیم که متابولیسم DNA مربوط به ویروس های پاپووا مانند SV40 و پولی ویروس ها، نسبت به متابولیسم مربوط به سلول های میزبانی که بوسیله ی این ویروس ها آلوده شده اند، متفاوت است. وقتی SV40 و پولی ویروس، سلول های میزبان را آلوده کند، DNA های ویروس به عنوان مولکول های خود مختار تکثیر می شوند. این تکثیر به صورت خارج کروموزومی، انجام می شود. هر دو ویروس، می توانند چند ده هزار ژنوم مدور با ساختار استاندارد دوتایی DNA تولید کنند که اندازه ی آنها 5 kb یک ژنوم ویروس منفرد است که بوسیله ی عفونت ایجاد می شود. در حالی که تکتثیر DNA ی مربوط به ویروس موجب ایجاد آنزیم های تقسیم سلولی خاص در سلول میزبان می شود، این مسئله موجب آلودگی در کروموزوم سلول آلوده و بنابراین، آلودگی در تقسیم سلولی می شود.
این تکرار غیر کروموزومی که در طی سیکل های لیتیکی مربوط به SV40 و ویروس پلیوما ایجاد می شود، هیچ اطلاعاتی در مورد نحوه ی تداوم این ژنوم های ویروسی در جمعیت های سلولی آلوده با ویروس، ارائه نمی دهد.
یک راه حل این پازل در سال 1968 منتشر شد. در این سال، کشف شد که DNA ویروس در سلول های آلوده شده با Sv40 به DNA کروموزومی آنها وابسته است. استفاده از روش های گریز از مرکز برای بررسی وزن های مولکولی مربوط به مولکول های DNA، نشان داد که DNA مربوط به ویروس SV40 در این سلول ها، دیگر مشابه با یک ژنوم ویروس DNA نیست. در عوض، توالی های DNA در ویروس SV40 که در داخل سلول های آلوده، قرار دارند، با DNA ی کروموزومی مربوط به سلول میزبان، اشتراک ایجاد می کند (شکل 4). در حقیقت، DNA ویروسی در این سلول های آلوده، نمی توانند از DNA کروموزومی سلول، جدا شوند. این کار با استفاده از روش های جداسازی خاص هم قابل انجام نیست.
برخی از رتروویروس ها به طور طبیعی آنکوژن حمل می کنند
توصیف مباحث مربوط به رتروویروس ها نشاندهنده ی این است که آنها ضرورتاً در دو گروه طبقه بندی می شوند. برخی از رتروویرس ها، مانند ALV و MLV هیچ آنکوژنی حمل نمی کنند، اما می توانند تومورهایی ایجاد کنند که تنها بعد از یک دوره ی زمانی نسبتاً طولانی، بروز می کنند. سایر ویروس ها مانند RSV می توانند به طور سریع موجب بروز سرطان شوند.در واقع، یک گروه سوم از رتروویروس ها وجود دارند که خواص متفاوتی دارد. ویروس لوسمی سلول T (HTLV-I) در حدود 1 % از ساکنین کیوشو (یکی از جزایر جنوب ژاپن) را آلوده کرده اند. یک عفونت بومی، نیز وجود دارد، البته با فراوانی کمتر، این مورد در جزایر کاراییب، مشاهده می شود. عفونت HTLV-I طولانی مدت، منجر به بروز 3 تا 4 % ریسک بروز لوسمی سلول T می شود.
برای بررسی مکان های تجمع این پروویروس ها در نواحی کروموزومی خاص، هیچ شاخصی وجود ندارد به جز بررسی های مولکولی گسترده. با توجه به این مسئله، این فهمیده شده است که برخلاف این مورد، HTLV-I از طریق جهش زایی، موجب بروز لوسمی می شود.
استفاده از مطالب این مقاله، با ذکر منبع راسخون، بلامانع می باشد.
/ج