قانون
در فیزیک، جرم به عنوان یک سیستم بسته یا مجزا شده شناخته میشود، به این معنی که تبادل ماده با محیط اطراف انجام نمیشود. بنابراین، به حالت تعادل ترمودینامیکی دست مییابد، به طوری که هیچ شکلی از مواد را نمیتوان از آن خارج یا به داخل آن حمل کرد. بر اساس این اصل، این قانون این گونه تعریف شده است:"جرم مواد در یک سیستم بسته یا مجزا شده، بدون توجه به این که چه فرآیندهایی در داخل سیستم صورت میگیرد، ثابت خواهد ماند." این بسیار شبیه به قانون بقای انرژی است که بیان میکند: "مقدار کل انرژی در یک سیستم مجزا شده با گذشت زمان ثابت میماند."
پیامد مشترک دیگر این دو قانون این است که هم جرم و هم انرژی نمیتوانند ایجاد شوند یا از بین بروند، بلکه فقط میتوان آنها را از یک حالت به حالت دیگر تبدیل کرد. براساس این قانون گفته میشود که جرم در طبیعت همیشه ثابت است اما میتواند در انواع مختلف ذرات و مراحل ماده تغییر فرم دهد. این قانون جدا از این که در بخش فیزیکی علم مورد استفاده قرار میگیرد، همچنین در واکنشهای شیمیایی که در سیستمهای بسته اتفاق میافتد، اعمال میشود، جایی که جرم واکنش دهندهها و محصولات باید برابر باشند.
مثالها
همان طور که در بالا ذکر شد، طبیعت پر از جرم است که به این یا آن شکل حفظ میشود. بنابراین، مثالهای زیادی وجود دارد که میتوانند برای تبیین این اصل در طبیعت مورد استفاده قرار بگیرند. برخی از سادهترین مثالها در زیر ذکر شده است؛ به این ترتیب میتوانید نحوه اعمال این قانون در زندگی روزمره را بیاموزید.شماره 1
هنگامی که ذغال سنگ را میسوزانید، محصولاتی وجود خواهد داشت که به دلیل این سوزاندن تشکیل میشوند، که دوده، خاکستر، گرما و انواع مختلفی از گازها هستند. اکنون این محصولات احتراق به طور مستقیم با مواد اولیه و یا زغال سنگِ موضوع سوختن متناسب هستند، به گونهای که ذغال سنگ به تمام این محصولات تبدیل شده است و این ثابت نگه داشته شدن جرم است. با این حال، هنگامی که جرم تبدیل میشود، انرژی گرمایی کمی تولید میکند. اما این تغییر بسیار جزئی است و به راحتی قابل تشخیص نیست، و بنابراین در نظر گرفته نمیشود.شماره 2
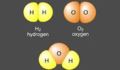
در این مثال، ما از یک واکنش شیمیایی بسیار اساسی بین یک مولکول (دو اتمی) هیدروژن با نیم مولکول (دو اتمی) اکسیژن بحث خواهیم کرد. هنگامی که این دو تحت گرما واکنش میدهند، یک مولکول آب (H2O) میدهند. جرم مواد در یک سیستم بسته یا مجزا شده، بدون توجه به این که چه فرآیندهایی در داخل سیستم صورت میگیرد، ثابت خواهد ماند. جرم اتمی هیدروژن 1 و جرم اتمی اکسیژن 8 است که هنگام ترکیب دو اتم هیدروژن و یک اتم اکسیژن 10 واحد تولید میشود که این وزن مولکولی آب است. بنابراین، در شیمی، جرم واکنش دهندهها در محصولات ثابت نگه داشته میشود.اطلاعاتی درباره قانون بقای جرم - انرژی
قبلاً در اواسط قرن هفدهم میلادی، میخائیل لومونوسف ابتدا ایدههای این قانون را آغاز کرد و شیمی را به دنیای واقعی علم معرفی کرد. بعداً، در سال 1789، ابتدا این قانون توسط یک دانشمند فرانسوی، آنتوان لاووازیه - مبتکر فیزیک مدرن - ترسیم شد. این قانون در گذشته به عنوان حفظ ماده یا اصل جِرم شناخته میشد. حال با دو جمله قابل توضیح است:1- یک سیستم کاملاً مجزا شده (سیستم بسته) را در نظر بگیرید. جرم چنین سیستمی در طی یک دوره زمانی ثابت خواهد ماند. فرآیندهای خاصی در داخل یک سیستم اتفاق میافتد و به این ترتیب جرم سیستم بسته، راکد یا بدون تغییر میماند.
2- هیچ سیستمی در طبیعت وجود ندارد که کاملاً بسته یا جدا از محیط خارجی باشد. بنابراین جرم یک سیستم نه میتواند ایجاد شود و نه میتواند از بین برود. فقط امکان تغییر آن به ذرات مختلف یا انتقال آن به چندین شکل گرما و نور وجود دارد یا می تواند در فضا تنظیم مجدد شود.
بنابراین، قانون در مورد تغییرات شیمیایی خاص اعمال میشود. با توجه به توضیحی که در بالا گفته شد، ما میتوانیم قانون را با یک جمله ساده تعریف کنیم:
"در طی هر تغییر شیمیایی یا فیزیکی؛ کل جرم کلیه واکنش دهندههای موجود در واکنش شیمیایی برابر است با جرم کل محصولات در همان واکنش."
به عنوان مثال ، این معادله اکسید جیوه را در نظر بگیرید:
6ر92 گرم جیوه به اضافه 4ر7 گرم اکسیژن، میدهد 100 گرم اکسید جیوه
تک تک اتمهای جیوه و اکسیژن، که در شروع واکنش وجود دارند، هنوز هم به طور دقیق در انتهای واکنش، به شکل ترکیب اکسید جیوه موجود هستند. از این رو معادله قانون فوق به اندازه کافی توجیه میشود.
از آن جا که ما معادله و قانون را بیان کردیم، بیایید اظهاراتی را که در مطالب فوق بیان شد، بر اساس انرژی با قرار دادن آن در یک تعریف مناسب اجرا کنیم.
قانون بقای انرژی: "در طی یک واکنش شیمیایی، مقدار کل انرژی در سیستم بدون تغییر باقی میماند. این بدان معنی است که انرژی نه میتواند ایجاد شود و نه از بین میرود بلکه میتواند از یک شکل به شکل دیگر منتقل شود. "
از همهی قوانینی که در بالا گفته شد، یک چیز کاملاً واضح است که ،
مقدار کل ماده و انرژی موجود در کل جهان، مقداری ثابت است و هرگز نمیتواند کم و بیش تغییر کند.
این بخشی بود که آلبرت انیشتین در زمینه شیمی و علوم به طور کلی نقشی انقلابی در آن ایفا کرد. او مردی بود که معادله E = mc2 را کشف کرد و به تبع آن هر دو این قانون را در "تئوری نسبیت" خود ادغام کرد، که تعریف قانون را کاملاً تغییر داد. وی این امکان را فراهم کرد که نشان دهد ماده و انرژی از یک شکل به شکل دیگر قابل تبدیل هستند. پس از آن، امروز، این دو قانون جداگانه با عنوان قانون بقای انرژی - جرم شناخته میشود.
منبع: Aparna Jadhav - ScienceStruck